반응 :
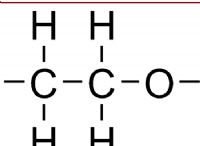
cu +o (s) + h₂so₄ (aq) → cuso₄ (aq) + cu (s) + h₂o (l)
설명 :
* 산화 환원 반응 : 이 반응은 산화 환원 반응이며, 이는 전자가 반응물 사이에 전달됨을 의미한다. 구리 (I) 산화물은 구리 금속 (Cu)으로 감소되는 반면, 구리 (I) 이온 중 일부는 구리 (II) 설페이트 (CUSO₄) 중 구리 (II) 이온 (Cu²⁺)으로 산화된다.
* 산-염기 반응 : 산-염기 반응도 발생합니다. h assots는 산으로서 작용하여, 양성자 (h⁺)를 cu₂O로부터 산화물 이온 (o²⁻)에 기증한다. 이것은 물을 형성합니다 (h (o).
* 불균형 : cu₂o의 구리 (I) 이온 (cu⁺)은 불균형 반응을 겪는다. 이는 산화되고 감소된다.
* 일부 큐 이온은 쿠소에서 cu² ⁺ 이온으로 산화됩니다.
* 다른 cuions 이온은 Cu 금속으로 감소됩니다.
전반적으로 반응은 다음과 같습니다.
* 구리 (II) 설페이트 (cuso₄) :이것은 용액에 용해 된 가용성 이온 성 화합물입니다.
* 구리 금속 (Cu) :이것은 용액에서 침전 될 수있는 적갈색 고체입니다.
* 물 (h>o) :이것은 액체 제품입니다.
중요한 메모 :
* 반응은 종종 반응을 용이하게하기 위해 열에서 수행됩니다.
* 반응의 정확한 화학량 론은 조건에 따라 다를 수 있습니다. 예를 들어, 황산이 농축 된 경우, 반응은 부산물로서 이산화황 (SO₂) 가스를 생성 할 수있다.
* 과량의 황산의 존재는 형성되는 황산염을 용해시키는 데 도움이되며, 용액을 파란색으로 보이게한다.
더 이상 질문이 있으면 알려주세요!