* 원자 번호 : 원자 수는 원자의 핵에서 양성자의 수를 나타냅니다. 수소에는 하나의 양성자가 있습니다.
* 전자 구성 : 지면 상태의 수소 원자는 1s 궤도에 하나의 전자를 가지고 있습니다. 이 구성은 가장 낮은 에너지 수준을 채우므로 안정적입니다.
* 짝을 이루지 않은 전자 : 수소의 단일 전자는 1s 궤도를 차지하며 자체 스핀과 쌍을 이룹니다. 짝을 이루지 않은 전자의 부족은 그 안정성에 기여합니다.
그러나 주목하는 것이 중요합니다.
* 동위 원소 : 가장 일반적인 수소 동위 원소 (양성자)는 하나의 양성자와 하나의 전자를 가지지 만, 중수소 (하나의 양성자, 하나의 중성자, 하나의 전자) 및 삼중 수소 (하나의 양성자, 2 개의 중성자, 하나의 전자)와 같은 다른 동위 원소가 있습니다. 이 동위 원소도 안정적입니다.
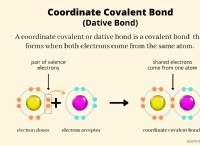
* 화학 반응성 : 지면 상태에서는 안정적이지만 수소는 여전히 반응성이 높습니다. 보다 안정적인 전자 구성을 달성하기 위해 다른 원자와 쉽게 결합을 형성합니다.
요약하면, 하나의 양성자 및 하나의 전자를 갖는 수소 원자는 전자 껍질이 채워지고 짝을 이루지 않은 전자의 부족으로 인해 안정적으로 간주된다. 그러나, 그 반응성은 다른 원자와 안정적인 결합을 형성 할 수있게한다.