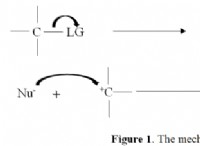
이유는 다음과 같습니다.
* 전자 구성 : 산소는 전자 구성 1s² 2s² 2p⁴ 인 반면 황은 1S² 2S² 2P⁶ 3S² 3P⁴을 갖는다.
* 차폐 : 황의 3S 및 3P 전자는 채워진 2S 및 2P 궤도에 의해 핵에서 차폐된다. 이 차폐는 원자가 전자에 의한 효과적인 핵 전하를 감소시킨다.
* 거리 : 황의 원자가 전자는 산소의 원자가 전자보다 핵으로부터 더 멀다.
* 전자-전자 반발 : 황의 외부 껍질에있는 전자의 수가 많을수록 전자-전자 반발이 더 커져 전자를 쉽게 제거 할 수 있습니다.
따라서 따라서 산소보다 황에서 전자를 제거하기 위해 에너지가 적습니다. 이것은 황이 첫 번째 이온화 에너지가 낮다는 것을 의미합니다.
이온화 에너지 또는 원자 구조와 관련된 다른 개념에 대한 자세한 내용을 원하시면 알려주십시오!