화학의 염기 및 산 정의 :
화학에는 산과 염기에 대한 여러 가지 정의가 있으며 각각 고유 한 초점과 범위가 있습니다. 다음은 세 가지 일반적인 정의입니다.
1. Arrhenius 정의 :
* 산 : 물에 용해 될 때 수소 이온 (H+)을 생성하는 물질.
* 베이스 : 물에 용해 될 때 수산화물 이온 (OH-)을 생성하는 물질.
예 :
* HCl (염산) :HCL → H + + CL-
* naoh (수산화 나트륨) :naoh → Na + + OH-
2. Brønsted-Lowry 정의 :
* 산 : 양성자 (H+)를 기증하는 물질.
* 베이스 : 양성자 (H+)를 받아들이는 물질.
예 :
* HCl (염산) + H2O (물) → H3O + (Hydronium 이온) + Cl- (클로라이드 이온)
* HCl은 물에 양성자를 기증하기 때문에 산입니다.
* 물은 HCl에서 양성자를 받기 때문에 기저입니다.
3. 루이스 정의 :
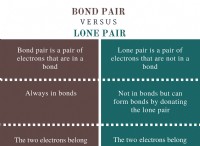
* 산 : 전자 쌍을 받아들이는 물질.
* 베이스 : 전자 쌍을 기증하는 물질.
예 :
* BF3 (붕소 트리 플루오 라이드) + NH3 (암모니아) → F3B-NH3
* BF3는 암모니아의 전자 쌍을 받아들이 기 때문에 산입니다.
* NH3은 전자 쌍을 붕소 트리 플루오 라이드에 기부하기 때문에베이스입니다.
키 포인트 :
* Arrhenius 정의는 물에 용해되는 물질로 제한됩니다.
* Brønsted-Lowry 정의는 더 넓고 비-수성 용매의 반응을 포함합니다.
* Lewis 정의는 양성자 전달과 관련이없는 가장 광범위한 반응입니다.
올바른 정의 선택 :
정의 선택은 특정 컨텍스트에 따라 다릅니다. Arrhenius 정의는 물의 간단한 산-염기 반응에 유용한 반면, Brønsted-Lowry 정의는 더 일반적이며 더 넓은 범위의 반응에 적용 할 수 있습니다. Lewis 정의는 산베이스 반응을 이해하기위한 가장 포괄적 인 프레임 워크를 제공합니다.