1. 화학 기호 이해
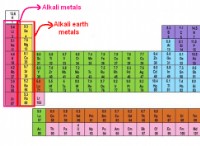
* 요소 기호 : 기호 자체 (예 :탄소의 경우, O 산소의 경우)는 요소를 알려줍니다.
* 원자 번호 (z) : 기호 앞의 첨자 번호는 원자 번호를 나타냅니다. 이것은 핵의 양성자 수입니다.
* 질량 수 (a) : 기호 앞의 슈퍼 스크립트 번호는 질량 번호를 나타냅니다. 이것은 핵의 총 양성자와 중성자 수입니다.
* 충전 : 기호 다음과 같은 슈퍼 스크립트는 이온의 전하를 나타냅니다. 양성 (+)이라면 이온은 전자를 잃었습니다. 부정적인 (-)이면 전자를 얻었습니다.
2. 입자 수 계산
* 양성자 : 양성자의 수는 원자 수 (z)와 같습니다.
* 중성자 : 중성자 수는 질량 수 (a)에서 원자 수 (z)를 빼서 계산됩니다. a -z =중성자 수.
* 전자 :
* 중성 원자 : 전자의 수는 양성자 수 (z)와 같습니다.
* 이온 :
* 양이온 (양전하) : 원자 번호 (z)에서 전하를 빼십시오. 예를 들어, +2 전하는 양성자보다 2 개의 전자가 적습니다.
* 음이온 (음전하) : 원자 번호 (z)에 전하를 추가하십시오. 예를 들어, -2 전하는 양성자보다 2 개의 전자를 의미합니다.
예 :산소 이온 (O²⁻)
* 요소 : 산소
* 원자 번호 (z) : 8
* 질량 수 (a) : 16 (가장 일반적인 동위 원소를 가정)
* 충전 : 2-
* 양성자 : 8 (원자 번호와 동일)
* 중성자 : 16-8 =8
* 전자 : 8 (원자 번호) + 2 (전하) =10
다른 예를 통해 작업하고 싶다면 알려주세요!