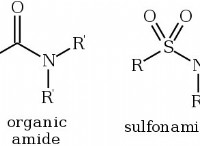
* 원자가 : 수소 (H)는 1 개의 원자가 전자를 가지며 산소 (O)는 6을 가지고 있습니다. 안정적인 화합물을 형성하려면 외부 껍질을 완성하기 위해 전자를 공유해야합니다.
* 본딩 : 산소는 안정적인 낙지를 달성하기 위해 2 개의 더 많은 전자가 필요하지만 수소는 하나가 필요합니다. 따라서, 안정적인 화합물은 하나의 산소 원자와 결합하는 2 개의 수소 원자와 형성되어 h₂o 를 초래할 것이다. .
vsepr h₂o
* 중앙 원자 : 산소
* 본딩 쌍의 수 : 2 (각 수소에 하나)
* 고독한 쌍의 수 : 2 (산소 원자에서)
VSEPR 이론에 따르면,이 배열은 구부러진 또는 각도 분자 형상 로 이어진다. 결합 각은 약 104.5도입니다.
다른 화학 질문이 있으면 알려주세요!