1. 용해도 이해
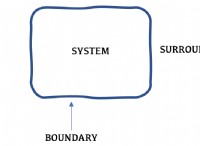
* 용해도 : 특정 온도에서 주어진 양의 용매에 용해 될 수있는 최대 양의 물질 (용질).
* ksp : 용해도 생성물 상수, 고체 이온 성 화합물과 그의 용해 된 이온 사이의 평형을 나타내는 값은 포화 용액.
2. 바륨 설페이트 용해도 제품
황산 바륨의 KSP는 1.1 x 10
Baso
ksp =[ba
2+
] [so 4
3. 용해도 계산
'' '는 Baso 4 의 어금니 용해도를 나타냅니다 . 평형에서 :
* [ba
2+
] =s
* [so 4
KSP 표현으로 대체 :
s * s =1.1 x 10
s
2
=1.1 x 10
-10
s =√ (1.1 x 10
4. PPM으로 변환
* Baso 4의 몰 질량 : 233.38 g/mol
* 1 ppm =1 mg/l
1.05 x 10
따라서 황산 바륨의 용해도는 약 2.45 ppm입니다.
중요한 참고 : 이것은 이론적 계산입니다. 실제 용해도는 용액에서 온도, pH 및 다른 이온의 존재와 같은 인자에 따라 약간 달라질 수 있습니다.