1. 압력 :
* 직접 비례 : 압력이 높을수록 CO2가 액체에 더 많이 용해됩니다. 이것이 바로 소다 병에 압력을 가하는 이유입니다. 병을 열면 압력이 감소하고 CO2가 탈출하여 피즈가 발생합니다.
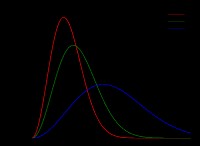
2. 온도 :
* 반비례 비례 : 온도가 증가함에 따라 CO2의 용해도가 감소합니다. 이것이 바로 소다가 냉장고보다 실온에서 더 빨리 평평하게됩니다.
3. pH :
* 직접 비례 : 낮은 pH (더 산성)는 CO2의 용해도를 증가시킨다. 이는 CO2가 물과 반응하여 탄산산 (H2CO3)을 형성 한 다음 수소 이온 (H+) 및 중탄산염 이온 (HCO3-)으로 분리하기 때문입니다. 수소 이온의 존재는 평형을보다 탄산의 형성으로 이동시켜 CO2 용해도가 높아집니다.
4. 감미료 :
* 사소한 효과 : 당 및 다른 감미료는 CO2의 용해도를 약간 감소시킬 수 있지만, 그 효과는 압력 및 온도에 비해 비교적 작습니다.
5. 다른 성분 :
* 사소한 효과 : 구연산, 향료 및 방부제와 같은 소다의 특정 성분은 CO2 용해도에 약간의 영향을 줄 수 있습니다.
6. 표면적 :
* 소다의 제한 효과 : 액체와 가스 사이의 더 큰 표면적 접촉 면적은 일반적으로 용해도를 증가시킬 것이지만, 밀봉 된 소다 병에서는 그 효과가 무시할 수 있습니다.
요약 :
소다에서 CO2 용해도에 영향을 미치는 가장 중요한 요소는 압력 및 온도 입니다. . 온도를 낮추고 압력을 높이는 것이 최대 CO2 보유 및 기교를 보장하는 주요 방법입니다.