분자 내 수소 결합의 중요성 :
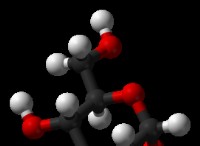
* 살리실산 (2- 하이드 록시 벤조산) : 2- 위치의 하이드 록실기 (OH)는 카르 복실 그룹 (COOH)과 강한 분자 내 수소 결합을 형성 할 수있다. 이 상호 작용은 탈 양성자 화 후 형성된 카르 복실 레이트 음이온 (쿠-)을 안정화시킨다. 음이온의 안정성으로 인해 양성자를 잃어 버릴 수있어 산도가 높아집니다.
* 4- 하이드 록시 벤조산 (P- 하이드 록시 벤조산) : 4- 위치의 히드 록실기는 너무 멀리 떨어져 카르 복실 그룹과 분자 내 수소 결합을 형성하기에는 너무 멀다. 결과적으로, 카르 복실 레이트 음이온은 덜 안정화되고 산은 덜 산성이다.
요약 :
산도의 주요 차이는 하이드 록실기가 카르 복실 그룹과 안정화 내 분자 내 수소 결합을 형성하는 능력에있다. 이 상호 작용은 살리실산에 존재하지만 4- 하이드 록시 벤조산에는 없다.
유기 화학에 대해 더 이상 질문이 있으면 알려주세요!