1. 기본 이해
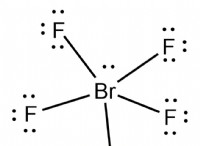
* 불소 (f) : 불소는 주기성 테이블의 그룹 17 (VIIA)에 있으며, 이는 7 개의 원자가 전자가 있음을 의미합니다.
* 수소 (H) : 수소에는 1 개의 원자가 전자가 있습니다.
* 공유 결합 : HF에서, 수소 및 불소는 전자를 공유하여 공유 결합을 형성한다.
2. 전자 구성
* 중성 불소 : 중성 불소 원자의 전자 구성은 1S² 2S² 2p⁵입니다.
* HF의 불소 : 불소가 수소와 결합을 형성하면 수소로부터 전자를 얻습니다. 이것은 가장 바깥 쪽 쉘 (2p 궤도)을 완성하여 1s² 2s² 2p⁶의 전자 구성을 제공합니다. 이것은 고귀한 가스 네온 (NE)과 동일한 전자 구성이므로 매우 안정적입니다.
따라서, HF의 F 원자는 네온 (NE)의 전자 구성에 도달합니다.