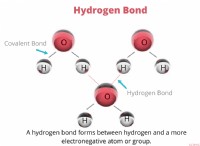
용해도 이해
* 가용성 화합물 : 이들은 용매 (보통 물)에 쉽게 용해되어 용액을 형성합니다. 그들은 이온으로 분리되어 용매 분자로 둘러싸여 있습니다.
* 불용성 화합물 : 이들은 용매에 크게 녹지 않습니다. 그들은 고체 입자로 남아 있습니다.
불용성 화합물의 형성
불용성 화합물은 몇 가지 메커니즘을 통해 형성 될 수 있습니다.
1. 강수 반응 :
* 혼합 솔루션 : 가용성 화합물을 함유하는 용액을 혼합하면 때때로 이온이 결합되어 불용성 화합물을 형성합니다.
* 고체의 형성 : 이 불용성 화합물 인 침전물 , 용액과 분리되어 고체로 나타납니다.
* 예 : 염화나트륨 (NaCl, 가용성)의 용액과 질산은 (Agno₃, 가용성)의 용액을 혼합하면 백색 침전물로서 염화은 (AgCl, 불용성)을 형성합니다.
2. 조건의 변화 :
* 온도 : 일부 화합물의 용해도는 온도에 따라 크게 변합니다. 용액을 가열하면 때때로 가용성 화합물이 용해성이 떨어지고 침전 될 수 있습니다.
* pH : 용액의 산도 (pH)를 변경하면 화합물의 용해도에 영향을 줄 수 있습니다.
* 용매 : 용매를 변경하면 용해도에도 영향을 줄 수 있습니다. 물에 용해 된 화합물은 알코올과 같은 다른 용매에서 불용성 일 수 있습니다.
키 포인트
* 용해도 규칙 : 화학자들은 용해도 규칙을 개발하여 어떤 화합물이 물에 용해되거나 불용 할 것인지 예측했습니다. 이 규칙은 관련된 이온의 유형을 기반으로합니다.
* 평형 : 강수 반응은 종종 가역적입니다. 불용성 화합물의 형성은 고체가 안정적인 지점에 도달 할 때까지 고체가 계속 용해되고 개혁되는 평형 공정이다.
예
불용성 화합물이 어떻게 형성되는지에 대한 다른 예는 다음과 같습니다.
* 탄산 칼슘 (카코) 형성 : 껍질과 석회암에서 발견되는이 불용성 화합물은 해수에서 칼슘 이온 (Ca²⁺) 및 탄산염 이온 (Co₃²⁻)의 반응으로부터 형성됩니다.
* 철 황화물 (FES) 형성 : 이 검은 불용성 화합물은 철 이온 (Fe²⁺)이 황화물 이온 (S²⁻)과 반응 할 때 형성됩니다.
이 예를 살펴 보거나 용해도와 강수량에 대해 더 많은 질문이 있으시면 알려주십시오!