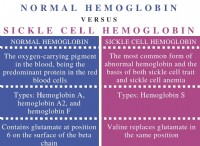
1. 극성과 매력
* 물 (HATER)은 극성 분자입니다 : 전자의 고르지 않은 공유로 인해 약간 양의 끝 (수소)과 약간 음의 끝 (산소)이 있습니다.
* 소금 (NaCl)은 이온 성 화합물입니다 : 그것은 긍정적으로 하전 된 나트륨 이온 (na⁺)과 음으로 하전 된 클로라이드 이온 (Cl⁻)으로 만들어졌습니다.
2. 용해 과정
* 매력 : 물 분자의 양의 끝은 염의 음성 클로라이드 이온 (Cl⁻)에 끌린다. 유사하게, 물 분자의 음성 끝은 양성 나트륨 이온 (Na⁺)에 끌린다.
* 주변 : 이 관광 명소는 물 분자가 개별 이온을 둘러싸고 소금 결정에서 멀어지게합니다.
* 분리 : 물 분자와 이온 사이의 강한 인력은 염 결정의 이온들 사이의 인력을 극복하여 소금이 분리되게한다 (해리).
3. 결과
* 용해 된 이온 : 분리 된 나트륨 및 염화물 이온은 물 분자로 둘러싸여있어 용액을 형성합니다. 물 분자는 본질적으로 이온을 "케이지"로, 이들을 재결합하고 다시 고체 결정을 형성하는 것을 방지한다.
시각화 :
자석처럼 생각하십시오. 물 분자는 작은 자석으로 작용하여 소금 결정에서 반대로 하전 된 이온을 끌어 당기고 당기는 것입니다. 물 분자는 효과적으로 이온을 둘러싸고 분리하여 고체 소금 결정을 다시 형성하지 못하게합니다.
키 포인트 :
* 용해도 : 물에 용해되는 소금의 양은 온도에 따라 다릅니다. 따뜻한 물은 용해 된 소금을 더 많이 담을 수 있습니다.
* 포화 : 물이 더 이상 소금을 녹일 수 없으면 "포화"라고합니다.
* 증발 : 물을 증발하면 용해 된 염 이온이 재결합하여 결정화되어 다시 염 결정이 형성됩니다.





![이번 토요일에 Mars Rover Launch Live를보십시오 [비디오 스트림]](/article/uploadfiles/202211/2022111014494262_S.jpg)