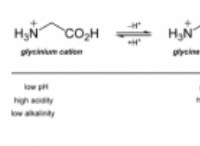
* 비등점 정의 : 액체의 끓는점은 증기압이 주변 대기압과 같은 온도입니다. 이 시점에서 액체는 가스로 전이됩니다.
* 순수한 물질 : 순수한 물질 (순수한 물 또는 순수한 에탄올)은 주어진 대기압 하에서 특정 끓는점을 갖는다. 이것은 물질 내의 분자가 서로에게 일관된 매력을 가지기 때문에이 매력을 극복하고 기화되기 위해 특정 양의 에너지 (열)가 필요하기 때문입니다.
* 혼합물 : 반면에 혼합물은 다르게 행동 할 수 있습니다. 혼합물은 둘 이상의 물질의 조합이다. 혼합물의 각 성분에는 고유 한 비등점이있을 수 있습니다. 이 경우, 혼합물은 일반적으로 두 개의 뚜렷한 비등점이 아닌 비등점 범위를 갖습니다.
* 예 : 바닷물은 혼합물입니다. 가열되면 물은 순수한 물보다 약간 더 높은 온도에서 끓기 시작합니다. 그러나 두 개의 뚜렷한 끓는점이 없습니다.
가능한 오해 :
* 분수 증류 : 이 기술은 서로 다른 끓는점에 따라 혼합물의 구성 요소를 분리하는 데 사용됩니다. 혼합물을 가열하고 가장 낮은 비등점을 갖는 성분이 먼저 기화되어 수집 할 수 있습니다. 이 과정은 다른 구성 요소를 분리하기 위해 반복 될 수 있지만 액체 자체에는 여전히 두 개의 비등점이 없습니다.
* 압력 변화 : 대기압의 변화는 액체의 끓는점에 영향을 줄 수 있습니다. 대기압이 낮은 높은 고도에서는 비등점이 감소합니다. 그러나 이것은 여전히 특정 조건 하에서 액체에 대한 단일 끓는점을 의미합니다.
요약하면, 순수한 액체는 주어진 압력 조건 하에서 단일 끓는점을 갖는다. 혼합물은 비등점 범위를 가질 수 있지만 두 개의 뚜렷한 끓는점을 가질 수는 없습니다.