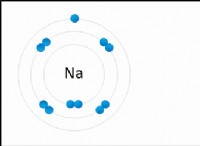
* 수소는 주기율표의 그룹 1 (또는 IA)에 있으며 알칼리 금속입니다. 이 그룹에는 리튬 (LI), 나트륨 (NA), 칼륨 (K), 루비듐 (RB), 세슘 (CS) 및 프랑크 (FR)와 같은 요소가 포함됩니다.
* 모든 알칼리 금속은 금속입니다. 이것은 그들이 열과 전기의 좋은 지휘자이며, 가단성 (모양이 될 수 있음)이며 연성 (전선으로 끌어들 수 있음)을 의미합니다.
그래서 수소가 특별한 이유는 무엇입니까?
* 수소는 다르게 행동합니다. 다른 알칼리 금속과는 달리, 수소는 실온에서의 가스이며, 규정 분자 (H2)로 존재하며 비 금속입니다.
* 수소의 전자 구성. 다른 알칼리 금속과 마찬가지로 하나의 원자가 전자를 가지고 있지만, 작은 크기와 높은 이온화 에너지로 인해 금속 특성이 부족합니다.
* 수소의 반응성. 때로는 알칼리 금속 (+1 이온 형성)처럼 작용하지만 일부 화합물에서 할로겐 (전자를 얻고 -1 이온을 형성)처럼 작용할 수 있습니다.
요약 : 수소는 독특한 요소이며 "금속"또는 "비금속"범주에 깔끔하게 맞지 않습니다. 알칼리 금속과 일부 특성을 공유하지만 그 행동은 더 미묘합니다.