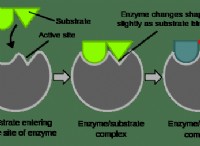
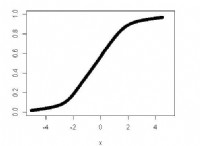
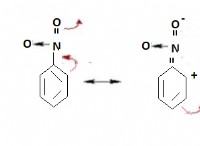
고귀한 가스 :
* 전체 원자가 껍질 : 고귀한 가스는 가장 바깥 쪽 바깥 쪽 전자 쉘을 가지고 있으며, 이는 에너지 수준이 보유 할 수있는 최대 전자 수가 있습니다. 예를 들어, 헬륨 (HE)은 가장 바깥 쪽 쉘에 2 개의 전자를 가지며, 이는 첫 번째 에너지 수준의 최대입니다.
* 안정적인 전자 구성 : 이 전체 쉘은 매우 안정적인 전자 구성을 생성하여 전자를 얻거나 잃기가 매우 어렵습니다. 그들은 이미 안정적이기 때문에 화학 반응에 쉽게 참여하지 않습니다.
다른 요소 :
* 불완전한 원자가 껍질 : 대부분의 다른 요소는 가장 바깥 쪽 바깥 쪽 전자 쉘을 가지고 있으므로 에너지 수준이 보유 할 수있는 것보다 전자가 적습니다.
* 안정성에 대한 욕망 : 이 요소들은 고귀한 가스와 같은 안정적인 전자 구성을 달성하기 위해 노력합니다. 그들은 이것을 달성 할 수 있습니다.
* 전자 얻기 : 비금속은 원자가 껍질을 채우기 위해 전자를 얻는 경향이 있으며, 음이온 (음이온)이됩니다.
* 전자 손실 : 금속은 전자를 잃는 경향이 있습니다. 전자가 원자가 껍질을 비워서 긍정적으로 하전 된 이온 (양이온)이됩니다.
* 화학 반응 : 전자를 얻거나 손실하기 위해, 원자는 다른 원자와 화학적 결합을 형성하여 분자 또는 이온 성 화합물의 형성을 초래한다.
예 :
* 나트륨 (NA) : 가장 바깥 쪽 쉘에 전자가 하나 있습니다. 안정적인 Na+ 이온을 형성하기 위해이 전자를 쉽게 잃어 버립니다.
* 염소 (CL) : 가장 바깥 쪽 껍질에 7 개의 전자가 있습니다. 안정적인 클리온을 달성하기 위해 하나의 전자를 쉽게 얻습니다.
* 나트륨과 염소 : 이들 원소는 나트륨이 전자를 잃고 염소가 전자를 얻는 안정적인 이온 성 화합물 인 염화나트륨 (NaCl)을 형성하기 위해 반응한다.
요약 : 고귀한 가스는 이미 안정적인 전자 구성을 가지고 있기 때문에 반응하지 않습니다. 다른 모든 요소는 불완전한 원자가 껍질을 가지고 있기 때문에 반응성이 있으며 전자를 얻거나 잃어버린 고귀한 가스 구성의 안정성을 달성하려고합니다.