원자 반경 추세 원자 반경 에 대해 설명합니다 요소의주기적인 테이블을 가로 질러 움직일 때 변경됩니다. 일반적으로 주기성 테이블에서 요소 그룹을 아래로 이동함에 따라 요소의 원자 반경이 증가하는 경향이 있습니다.
이것이 왜 발생하는지 이해하려면 주기율표에서 원자 반경의 정의와 다른 요소의 반경을 면밀히 살펴 보는 것이 도움이 될 것입니다.
원자 반경이란 무엇입니까?
원자 반경은 원자의 크기를 나타냅니다. 그러나이 가치는 생각만큼 쉽게 고정하는 것이 아닙니다. 우선, 원자 반경이라는 용어는 원자의 크기를 참조하는 데 사용되지만이 값에 대한 합의 된 정의는 없다는 사실을 알고 있어야합니다. 이온 반경, 금속 반경, 공유 반경 및 반 데르 발스 반경을 포함하여 원자 반경을 측정하는 다양한 방법이 사용됩니다.
이온 반경은 결정 격자에있을 때 원자의 이온의 척도를 말하며, 일반적으로 간신히 만지는 두 가지 이온의 핵 사이의 거리의 절반입니다. 공유 반경은 공유 결합의 일부를 구성하는 원자의 크기입니다. 금속 반경은 양으로 하전 된 금속 이온과 전도 전자 사이의 특정 유형의 화학적 결합을 나타냅니다. 금속 반경은 일반적으로 금속 격자에서 서로 인접한 두 금속 이온 사이의 거리의 절반으로 정의됩니다. 반 데르 발스 반경 반경은 정의 된 요소에서 두 개의 비 결합 원자의 가장 가까운 접근 사이에 존재하는 거리를 나타냅니다.
원자 반경 추세는 무엇입니까?
원자 반경은 여러 가지 다른 방식으로 정의 될 수 있지만 주기율표를 가로 지르는 일반적인 원자 반경 추세는 사실입니다. 요소의 원자에 대한 원자 반경은 테이블의 요소 그룹을 아래로 이동할 때 올라가는 경향이 있습니다. 테이블의 새 행에 새 전자 쉘이 원자에 추가되기 때문에 열을 아래로 이동함에 따라 원자 반경이 증가합니다.
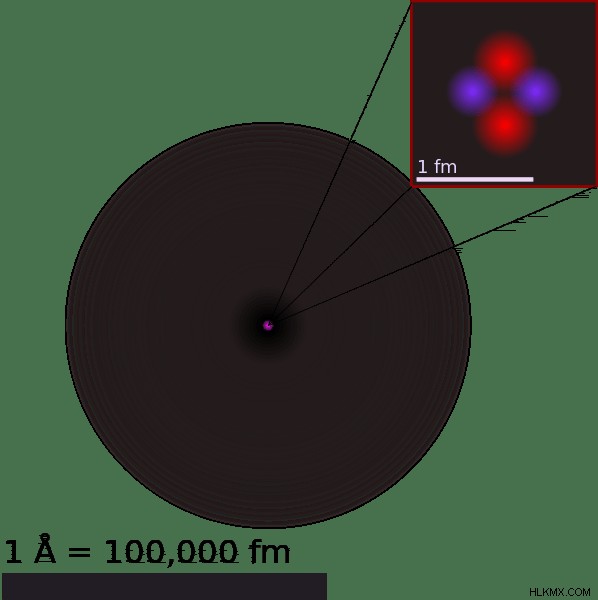
이에 대한 결론은 원자 수가 증가함에 따라 원자 당 더 많은 전자가 있기 때문에 원자 반경이 왼쪽에서 오른쪽으로 향할 때 감소 할 수 있다는 것입니다.
.
원자 반경은 어떻게 측정됩니까?
원자가 지속적으로 움직이고 있으므로 원자 반경의 측정 시도는 일정량의 오류가 내장되어 있음을 의미합니다. 원자 반경의 측정은 거의 만지지 않는 두 개의 다른 원자의 핵 사이의 거리를 측정하여 수행됩니다. 두 핵 사이의 거리의 직경은 반경을 얻기 위해 2로 나뉩니다. 원자 반경을 측정 할 때 측정되는 원자는 화학적 결합을 공유 할 수 없다는 것을 기억해야합니다. 화학적 결합은 원자의 전자 쉘이 겹치거나 외부 껍질을 공유한다는 것을 의미하기 때문입니다.
원자 반경과 이온 반경의 차이
이온 반경 및 원자 반경은 크립톤, 네온 및 아르곤과 같은 중성 원소의 모든 원자와 동일합니다. 그러나 많은 원자가 순 전하가있을 때 가장 안정적입니다. 실제로 이것은 가장 바깥 쪽 전자를 떨어 뜨릴 때 양이온 (양으로 하전 된 이온)이된다는 것을 의미합니다. 전자가 원자에서 떨어지면 원자는 종종 가장 바깥 쪽 전자 쉘을 떨어 뜨립니다. 이는 원자 반경을 이온 반경보다 크게 만드는 효과가 있습니다.
.
일부 원자는 양전하로 더 안정적이라는 사실과 달리, 일부는 순 음전하로 더 안정적입니다. 이 경우, 하나 이상의 전자를 얻어 음이온 (음으로 하전 된 이온)으로 변신하여 더 안정적이됩니다. 그러나 또 다른 전자 쉘은 추가되지 않으므로 이온 반경과 원자 반경의 크기 차이는 양이온에 존재하는 차이만큼 크지 않다는 것을 의미합니다. 이것은 원자 반경이 항상 이온 반경과 동일하거나 약간 작다는 것을 의미합니다. 일반적으로, 이온 반경의 추세는 원자 반경과 비슷한 경향을 가지며 주기율표를 가로 질러 움직일 때 크기가 증가합니다.
주기율표에서 발견 된 기타 트렌드
원자 반경 추세와는 별도로 주기율표에서 찾을 수있는 다른 트렌드가 있습니다. 주기율표에서 발견 된 다른 트렌드는 전기 음성 트렌드, 이온화 에너지 트렌드 및 전자 친화력 추세가 있습니다.
전기 음성 트렌드는 요소 섹션을 가로 질러 왼쪽으로 오른쪽으로 이동함에 따라 원자의 전기 음성 값이 증가한다는 사실을 반영합니다. 테이블의 그룹을 위에서 아래로 내려 가면서 전기 음성도 감소합니다. 전기 음성 경향에 대한 주목할만한 예외에는 Ianthanides, Actinides 및 고귀한 가스가 포함됩니다. 전이 금속은 그 안에 거의 차이가 없습니다.
이온화 에너지 추세는 기체 중성 원자에서 전자를 제거하는 데 필요한 이온화 에너지의 양이 주기율표를 가로 질러 어떻게 변하는지를 나타냅니다. 주기성 테이블의 오른쪽에있는 요소는 일반적으로 양이온이되기 위해 더 많은 이온화 에너지가 필요하지만 테이블의 왼쪽에있는 요소는 일반적으로 더 쉽게 양이온이됩니다. 다시 말해, 왼쪽에서 오른쪽으로 테이블을 가로 질러 이동함에 따라 이온화 에너지가 증가합니다.
전자 친화도 경향은 원자의 전자 친화력, 주어진 원자의 전자와 결합하는 능력을 추적한다. 원자의 전자 친화력 값이 낮을수록 원자가 전자를 쉽게 받아 들일 수 있습니다. 전자 친화력은 일반적으로 요소 그룹을 아래로 이동함에 따라 감소합니다. 주기적인 테이블 전자 친화력이 증가하는 왼쪽으로 오른쪽으로 이동하면
원자 반경의 예
원자 반경의 몇 가지 예를 살펴 보겠습니다. 이 원자 반경은 피코 미터로 측정됩니다 :
- 요소 수소 (H)의 원자 반경은 37입니다.
- 나트륨 (NA)의 원자 반경은 186입니다.
- 칼륨 (k)의 원자 반경은 227입니다.
- Rubidium (RB)의 원자 반경은 248입니다.
- 세슘 (CS)의 원자 반경은 265입니다.
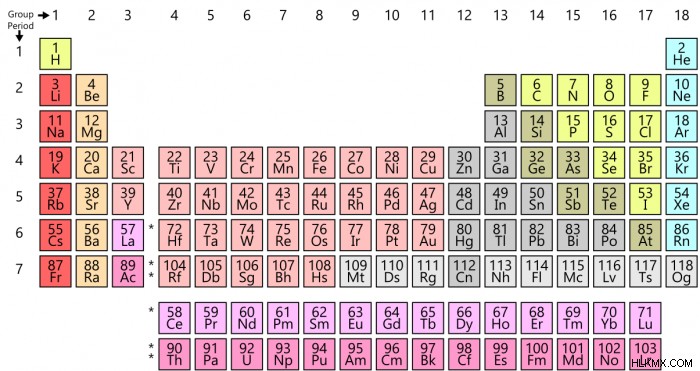
이 요소는 모두 주기성 테이블의 첫 번째 열에서 발견되며 내림차순으로 표시됩니다. 이것은주기적인 테이블을 아래로 이동할 때 원자 반경이 어떻게 증가하는지 깔끔하게 보여줍니다.