상태 :
* 고체 : 명확한 모양과 부피, 분자는 단단히 포장됩니다. 예 :암석, 얼음, 금속.
* 액체 : 확실한 볼륨이지만 용기의 모양을 취합니다. 분자는 느슨하게 포장됩니다. 예 :물, 기름, 수은.
* 가스 : 명확한 모양이나 부피가없고, 분자는 매우 느슨하게 포장되어 자유롭게 움직입니다. 예 :공기, 산소, 이산화탄소.
* 혈장 : 전자가 원자에서 벗겨져 이온과 전자의 혼합물을 생성하는 과열 가스. 예 :번개, 태양, 형광등.
구성에 의한 :
* 순수한 물질 : 단일 유형의 원자 또는 분자. 예 :금, 물, 산소.
* 혼합물 : 둘 이상의 순수한 물질이 함께 혼합되었습니다. 예 :바닷물, 공기, 토양.
* 요소 : 한 가지 유형의 원자로 만들어진 순수한 물질. 예 :탄소, 수소, 산소.
* 화합물 : 화학적으로 결합 된 둘 이상의 다른 원소로 만든 순수한 물질. 예 :물 (HATER), 이산화탄소 (CO₂).
속성에 의한 :
* 물리적 특성 : 물질의 화학적 조성을 변경하지 않고 관찰 할 수 있습니다. 예 :색상, 밀도, 녹는 점, 끓는점.
* 화학적 특성 : 물질이 다른 물질과 어떻게 반응하는지 설명하십시오. 예 :가연성, 산과의 반응성, 산화.
구조 별 :
* 원자 수준 : 물질은 요소의 가장 작은 단위 인 원자로 구성됩니다. 원자는 양성자, 중성자 및 전자로 만들어집니다.
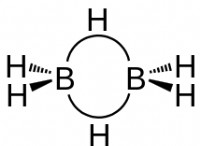
* 분자 수준 : 원자는 함께 결합하여 분자를 형성 할 수 있으며, 이는 화학적 결합에 의해 함께 유지되는 2 개 이상의 원자 그룹이다.
* 거시적 수준 : 이것은 육안으로 관찰 될 수있는 물질의 특성과 행동을 말합니다.
다른 접근법 :
* 위상 다이어그램 : 이는 물질이 다른 상태 (고체, 액체, 가스)에 존재하는 조건 (온도 및 압력)을 설명합니다.
* 분광학 : 물질과 전자기 방사선의 상호 작용을 분석하여 구성 및 구조를 식별합니다.
* 양자 역학 : 복잡한 수학적 모델을 사용하여 원자 및 아 원자 수준에서 물질의 행동을 설명합니다.
과학자들이 물질을 묘사하는 특정 방식은 대답하려는 질문에 달려 있습니다. 예를 들어, 화학자는 물질의 화학적 조성 및 특성에 중점을 둘 수 있지만 물리학자는 원자 구조와 행동에 중점을 둘 수 있습니다.