Dalton Atomic 모델은 John Dalton이 제안한 원자의 모델입니다. 이 모델은 질량 보존 법칙, 일정한 비율, 다중 비율 및 상호 비율을 기반으로했습니다. 모델은 원자가 더 이상 나눌 수없는 작은 불가분의 구형 물체라고 가정했다. 이 모델은 나중에 핵, 양성자 및 전자의 발견에 의해 반증되었습니다.
누군가가 자신의 지성의 구성과 한계를 넘어서 생각하는 것은 어렵지만, 다른 인간의 마음에 의해 상상되지 않은 것을 생각하는 사람은 천재의 뇌에 속하는 위업입니다. 그것이 바로 John Dalton이 한 일입니다. 달튼 원자 모델의 대부분은 반증되었지만, 그는 오늘날 우리가 축하하는 원자 이론의 토대를 마련한 사람으로 여겨지고 있습니다. Dalton Atomic Model에 뛰어 들기 전에 이전에 확립 된 원자 이론에 대한 간략한 개요를 봅시다.
.

(사진 크레딧 :Charles Turner/Wikimedia Commons)
원자 이론의 기본 법칙
우리가 가장 먼저 보게 될 것은 질량 보존 법칙 입니다. . 1789 년 Antoine Lavoisier가 설립 한 법률이었다. 대중 보존 법은 화학 반응 후 반응물의 질량과 생성물의 순 변화가 0이라고 말한다. 이것은 질량이 파괴되거나 만들어 질 수 없음을 의미합니다. 이것은 질량이 항상 화학 반응에서 일정하게 유지됨을 의미합니다. 일부 반응 동안 질량이 열 및 결합 에너지와 상호 연결 될 수 있다는 사실 때문에 나중에이 법에서 몇 가지 부정확성이 언급되었습니다.
두 번째 법칙은 끊임없는 비율의 법칙 입니다 . 일정한 비율의 법칙에 따르면 화합물이 깨질 때 구성 요소의 질량은 동일한 비율로 유지된다고합니다. 이 법의 중요성은 화합물의 질량이 화합물의 위치, 수득 된 위치 또는 화합물의 질량에 관계없이 동일한 비율에서 동일한 원소를 갖는다는 사실입니다.
다음 법은 여러 비율의 법칙입니다. 이것은 두 원소가 그들 사이에 둘 이상의 화합물을 형성 할 때, 각 화합물에서 두 번째 요소의 질량의 비율은 작은 정수의 형태로 발현 될 수 있다고한다. 법은 이전 두 법률을 연구 한 후 Dalton 자신이 제안했습니다.
네 번째이자 마지막 법칙은 상호 비율의 법칙, 입니다. 이것은 두 개의 다른 요소가 동일한 양의 세 번째 요소와 결합 될 때, 그들이하는 비율은 그들이 결합하는 비율의 동일하거나 다중 일 것이라고 말합니다. James Ritcher는 1792 년 에이 법을 제안했습니다.
John Dalton Atomic Model
제시된 위의 법률에 근거하여 Dalton은 물질의 근본적인 특성에 대한 그의 아이디어를 공식화했는데, 이것이 그가 원자의 개념을 생각해 낸 방법입니다. 위의 법을 연구 한 후 큰 조사를 한 후, 그는 다음과 같은 가정을 생각해 냈습니다.
- 물질은 atoms 이라는 매우 작은 입자로 만들어집니다 .
- 원자는 화학 반응 중에 (질량 보존 법칙에 근거하여) 생성하거나 파괴 할 수없는 불가분의 구조입니다.
- 특정 요소의 모든 원자는 물리적 또는 화학적 특성을 포함하여 모든 측면에서 유사합니다.
- 반대로, 다른 요소의 원자는 다른 특성을 나타내며, 질량과 다른 화학적 특성이 다릅니다.
- 주어진 화합물의 상대적 수와 원자의 종류는 항상 고정 비율에 따라 고정 된 비율입니다.
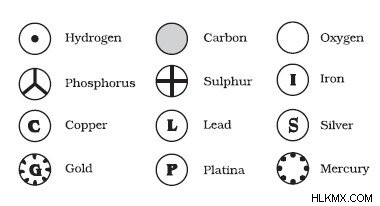 위의 추후 사항을 기반으로 Dalton은 Atom의 첫 번째 모델 중 하나를 제시 할 수있었습니다. 그의 모델의 또 다른 이름은 당구 공 모델입니다. 그는 원자를 더 이상 나눌 수없는 작은 불가분의 구형 대상으로 정의했다. 그는 당시 핵, 양성자 또는 전자의 개념에 대한 당시 (모든 사람과 마찬가지로) 알지 못했습니다. Dalton에게 원자를 그리라고 요청했다면, 그는 단순히 원을 그렸을 것입니다!
위의 추후 사항을 기반으로 Dalton은 Atom의 첫 번째 모델 중 하나를 제시 할 수있었습니다. 그의 모델의 또 다른 이름은 당구 공 모델입니다. 그는 원자를 더 이상 나눌 수없는 작은 불가분의 구형 대상으로 정의했다. 그는 당시 핵, 양성자 또는 전자의 개념에 대한 당시 (모든 사람과 마찬가지로) 알지 못했습니다. Dalton에게 원자를 그리라고 요청했다면, 그는 단순히 원을 그렸을 것입니다!
 그는 원자를 분류하려고 시도했으며 상징을 다른 요소에 할당 한 최초의 과학자였습니다. 그러나 그의 최선의 노력에도 불구하고 많은 불일치와 오류가 그의 이론의 기초에 들어갔다. bohr model 에 따라 원자가 양성자, 중성자 및 전자로 더 나눌 수 있기 때문에 두 번째 가정은 더 이상 받아 들여질 수 없습니다. 원자의. 동위 원소는 동일한 요소이지만 원자 구조가 다르기 때문에 세 번째 가정은 또한 거짓 인 것으로 밝혀졌습니다. 마지막으로, 네 번째 가정은 또한 동일한 질량을 가진 다른 요소의 원자 인 이소 바의 존재로 인해 잘못된 것으로 판명되었습니다.
그는 원자를 분류하려고 시도했으며 상징을 다른 요소에 할당 한 최초의 과학자였습니다. 그러나 그의 최선의 노력에도 불구하고 많은 불일치와 오류가 그의 이론의 기초에 들어갔다. bohr model 에 따라 원자가 양성자, 중성자 및 전자로 더 나눌 수 있기 때문에 두 번째 가정은 더 이상 받아 들여질 수 없습니다. 원자의. 동위 원소는 동일한 요소이지만 원자 구조가 다르기 때문에 세 번째 가정은 또한 거짓 인 것으로 밝혀졌습니다. 마지막으로, 네 번째 가정은 또한 동일한 질량을 가진 다른 요소의 원자 인 이소 바의 존재로 인해 잘못된 것으로 판명되었습니다.
J.J. 후 Thompson은 그의 원자 모델을 발표했으며 Dalton의 남은 가정에서 진실한 것을 강화했습니다. 나중에 Rutherford는 Dalton과 Thompson의 아이디어를 모두 결합하여 Atom에 대한 거의 정확한 모델을 제시했습니다. 마침내 Niels Bohr과 Quantum Mechanical 모델은 오늘날 우리가 알고 있고 존경하는 현대 원자 모델을 확립했습니다!