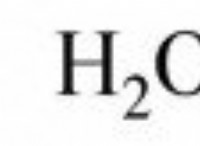화학에서, 강수 반응 하나 이상의 고체 제품을 형성하는 두 개의 용해 된 물질 사이의 화학 반응입니다. 고체는 침전물 입니다 . 나머지 솔루션은 Supernate 입니다 또는 상청액 .
표기법
화학 반응에서 강수량을 나타내는 두 가지 일반적인 방법이 있습니다.
- 물질의 상태 :화학적 공식을 따르는 기호를 포함하여 제품이 견고하다는 것을 의미합니다.
- 아래쪽 화살표 :그렇지 않으면 이름이나 공식의 아래쪽 화살표 (↓)는 침전물을 나타냅니다.
강수 반응이 작동하는 방법
침전은 용해도를 초과하는 화학 물질의 농도에서 비롯됩니다. 이런 일이 몇 가지 있습니다 :
- 이중 교체 반응 :종종 강수량은 두 수성 용액 사이의 이중 대체 반응으로 인해 발생합니다. 용해 된 염은 반응하고 하나 이상의 제품은 불용성 (또는 적어도 부분적으로 불용성)입니다.
- 결정화 :순수한 용액에서도 농도는 종종 용해도를 초과합니다. 입자는 핵 생성 단계 동안 집계되고 물질은 평형에 도달 할 때까지 용액이 떨어집니다. 온도와 압력을 제어하면 화학 물질이 용액을 벗어나게됩니다.
- 솔루션 변경 :화학 물질이 불용성되는 새로운 용매를 도입하면 종종 강수가 발생합니다. 이온을 추가하는 것은 또 다른 옵션이며, 응고를 향한 화합물을 유도하는 것입니다.
침전물을 형성하는 이중 대체 반응은 침전 반응이다. 침전물을 형성하는 다른 방법은 반응보다 더 많은 과정입니다.
모든 경우에, 강수량은 핵 생성으로 시작됩니다. 핵 생성 동안, 작은 입자는 서로에 부착되어 용기의 결함을 표면으로 지정합니다. 다른 핵 생성 부위는 용액 및 가스 기포의 고체 불순물을 포함한다. 초기에, 핵 생성은 액체에서 작은 고체 입자의 현탁액을 형성 할 수있다. 입자가 충분히 커지면 용액에서 침전하거나 떨어집니다.
침전 반응의 예
강수 반응의 일반적인 예는 다음과 같습니다. 강수 반응이 분자 방정식과 순 이온 방정식으로 보이는 방식에 주목하십시오. 반응을 쓰는 다양한 방법을 비교하십시오.
- 요오드화 칼륨과 질산염 사이의 반응으로 물에서 요오드화 리드를 형성하고 질산 칼륨으로 수성 칼륨을 형성합니다.
2ki (aq) + pb (no 3 )2 (aq) ⟶ pbi 2 (s) + 2kno 3 (AQ) (분자 방정식)
pb (aq)+2i (aq) ⟶pbi 2 (S) (순 이온 방정식)
- 물에서 불소 나트륨과 질산은 사이의 반응, 고체 은색 불소 및 질산 나트륨을 형성하는 것 :
NAF (aq) + agno 3 (aq) Agf (s) + nano 3 (AQ) (분자)
Ag (aq) + F (aq) ⟶ agf (들) (순 이온)
- 반응 구리 황산염 및 수산화 나트륨은 황산나트륨 및 수산화 구리를 형성합니다.
cuso 4 + 2naoh h na 2 그래서4 + Cu (OH) 2 ↓
- 황산나트륨과 클로라이드 스트론튬 사이의 반응은 염화나트륨과 황산 나트륨을 형성하며, 이는 압밀화입니다.
na 2 그래서4 + srcl 2 2NACL + srso 4 ↓
- 물에서 황산 카드뮴과 황화 칼륨 사이의 반응은 황산 칼륨과 황화 카드뮴을 형성합니다.
cdso4 (aq) + k 2 s (aq)) k 2 그래서 4 (AQ) + CDS (S)
일반적인 침전물 색상
침전물의 색은 그 정체성에 대한 단서입니다. 다음은 일반적인 전환 금속 침전물 색상입니다. 이 색상은 다른 화합물에서도 발생하며 이온의 산화 상태가 변하면이 화합물은 매우 다르게 보일 수 있습니다.
| 금속 | 색상 |
|---|---|
| Chromium | 블루, 녹색, 주황색, 노란색 또는 갈색 |
| 코발트 | 분홍색 (수화시) |
| 구리 | 블루 |
| 철 (II) | 녹색 |
| 철 (III) | 녹슬었던 붉은 갈색 |
| 망간 (II) | 옅은 분홍색 |
| 니켈 | 녹색 |