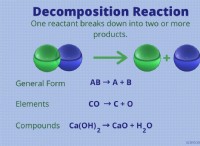
촉매 란 무엇입니까?
촉매가 무엇인지 이야기합시다. 촉매 화학적 반응 속도를 증가시키는 화합물 또는 요소입니다. 그 자체가 반응의 일부가되지 않고 발생하는 속도. 일반적으로 말하면, 촉매는 반응에서 파괴되거나 변하지 않습니다. 촉매는 활성화 에너지 을 낮추어이를 수행합니다 다음 섹션에서 설명하는
활성화 에너지 란 무엇입니까?
간단히 말해서, 활성화 에너지의 정의는 둘 이상의 원소 또는 화합물 사이의 반응을 시작하는 데 필요한 에너지입니다. 높은 활성화 에너지와의 반응은 천천히 진행될 수 있습니다. 속도를 높이거나 반응을 시작하려면 필요한 활성화 에너지를 추가 하거나이 요구 사항을 낮추는 촉매를 사용하여 반응의 속도를 높이십시오.
.활성화 에너지 단위는 에너지 단위 측면에서입니다. 사용되는 가장 일반적인 단위는 KJ/Mol 또는 J/Mol입니다.
입니다촉매는 어떻게 작동합니까?
촉매는 활성화 에너지를 감소시킴으로써 반응 속도를 증가시킨다. 활성화 에너지 감소는 반응을 시작하는 데 필요한 에너지가 줄어 듭니다.
아래 그래프는 촉매가 있거나없는 반응의 에너지를 보여줍니다. X 축은 반응물 (왼쪽)에서 생성물 (오른쪽)으로의 반응 좌표 또는 진행입니다. y 축은 에너지입니다.
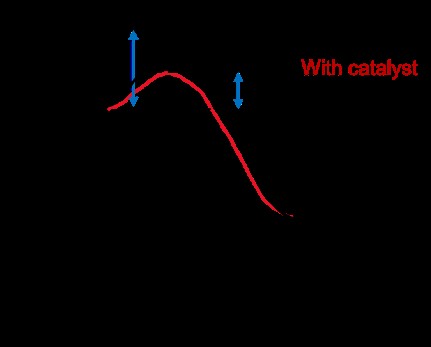
촉매가 존재함에 따라, 활성화 에너지 (e a ) 더 작습니다. 시각적으로, 반응이 내리막 길로 가기 전에 반응이 올라 가야하는 언덕은 더 작습니다. 작은 오르막길보다 자전거를 타는 것이 더 큰 오르막보다 쉬운 것처럼, 활성화 에너지 힐이 더 작을 때 반응이 더 빨리 진행됩니다.
촉매는 반응의 전이 상태를 변화시킴으로써 활성화 에너지를 낮 춥니 다. 그런 다음 반응은 촉매되지 않은 반응과 다른 경로/메커니즘을 통과합니다. 촉매는 반응물과 생성물 사이의 순 에너지 차이를 변화시키지 않습니다. 반응의 순 방정식은 전이 상태가 변하면 촉매 및 촉매되지 않은 반응에서 동일합니다.
전반적인 반응 :A + B + 촉매 -> AB + 촉매
순 반응 :a + b -> ab
촉매의 주요 범주
이종 촉매
이종 촉매는 반응물과 다른 단계에있다. 일반적으로, 이는 촉매가 고체에 있고 반응물은 액체 또는 기체상에 있음을 의미한다. 이종 촉매의 또 다른 이름은 표면 촉매입니다.
이종성 촉매는 촉매를 고체지지 구조에 부착하고 반응물이 촉매를 지나서 지나가는 길을 따라 반응함으로써 작용한다. 이러한 유형의 촉매의 이점은 반응이 완료 될 때 촉매가 생성물로부터 쉽게 분리된다는 것이다. 그런 다음 촉매를 쉽게 재사용 할 수 있습니다. 제조에서 이것은 중요한 비용 절감 척도입니다. 이종 촉매의 단점은 반응물과 촉매 사이의 상호 작용의 양이 표면적 및 표면으로부터 생성물의 확산에 의해 제한 될 수 있다는 것이다.
.일반적인 이종 촉매는 자동차의 휘발유를위한 촉매 변환기입니다. 또 다른 중요한 이종 촉매는 nh 3 를 형성하는 Haber-Bosch 공정입니다. .
균질 촉매
균질 한 촉매에서, 반응물과 촉매는 동일한 단계에있다. 일반적으로 그들은 액체 또는 기체상에 있습니다.
균질 한 촉매의 주요 이점은 반응물과 촉매 사이의 증가 된 상호 작용이다. 둘 다 자유롭게 움직일 수 있으므로 상호 작용하고 반응으로 이어질 가능성이 높습니다.
일반적인 균질 한 촉매는 전이 금속 및 산입니다. 하나의 균질 한 촉매 반응은 대기에서 산소를 오존으로 전환시키는 것입니다. 산화 질소 (NO)는 반응을 촉진시킨다. 반응의 모든 참가자는 기체상에 있습니다. 그러므로 우리는 그것이 균질 한 촉매 반응임을 알고 있습니다.
효소
효소는 생물학적 촉매 인 큰 단백질입니다. 그들은 몸의 강력한 힘입니다. 종종 그들은 하나의 매우 구체적인 반응 만 촉매합니다 (종종 훨씬 더 광범위한 반응을 촉매하는 무기 촉매와 비교할 때). 특이성은 촉매의 활성 부위에 기인합니다. 하나의 매우 특정 반응물 모델만이 맞는 아미노산에 의해 형성된 특정 화학 조성의 포켓에 기인합니다. 이것을 Lock-and-Key 모델이라고도합니다.
효소는 신체에서 많은 중요한 역할을합니다. 그들은 전분의 파괴를 촉매하여 포도당을 만듭니다. 그들은 또한 이산화탄소를 전환시킨다 (Co 2 ) 다른 분자들에게 hco 3 와 같은 신체 요구 . 효소는 신체의 거의 모든 과정을 돕고 촉진합니다.
활성화 에너지 계산
활성화 에너지 계산은 Arrhenius 방정식을 사용합니다. 기본 사항은 여기에서 다루어 지지만 더 많은 예와 심층 분석을 위해 Arrhenius 방정식 기사를 확인하십시오.
Arrhenius 방정식은 다음과 같습니다.
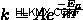
어디 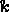 는 속도가 상수입니다.
는 속도가 상수입니다. 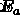 는 활성화 에너지입니다.
는 활성화 에너지입니다. 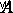 는 주파수 계수입니다.
는 주파수 계수입니다. 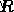 는 가스 상수입니다
는 가스 상수입니다 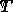 는 온도입니다.
는 온도입니다.
속도 상수를 알고 있다면 활성화 에너지를 찾을 수 있습니다 ( 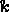 ).
). 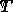 ). 활성화 에너지를 결정하기 위해 (
). 활성화 에너지를 결정하기 위해 ( 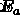 ) 우리는 플롯됩니다
) 우리는 플롯됩니다 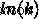 vs
vs 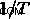 . 그렇게함으로써 우리는 경사면을 가진 선을 얻습니다.
. 그렇게함으로써 우리는 경사면을 가진 선을 얻습니다. 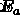 /
/ 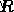 의 y 인터셉트
의 y 인터셉트 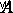 .
. 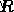 는 일정하므로 활성화 에너지를 해결할 수 있습니다.
는 일정하므로 활성화 에너지를 해결할 수 있습니다.
예를 들어 활성화 에너지 공식의 문제와 같은 문제는 Arrhenius 방정식 페이지를 참조하십시오!
공통 촉매 목록 :
- 바나듐 펜 옥사이드 (황산 만들기)
- 팔라듐 금속
- 이산화 망간
- 백금 금속 (촉매 변환기)
- 철 금속 (하버 과정에서)
- 클로라이드 알루미늄 (많은 유기 반응)
- 구리 (II) 산화물
- 효소 (생화학 반응에서 자연 발생 촉매)
촉매 및 활성화 에너지 어휘 정의
- 활성화 에너지 - 둘 이상의 원소 또는 화합물 사이의 반응을 시작하는 데 필요한 에너지
- 촉매 - 반응 속도를 증가시키고 반응에서 소비되지 않는 분자
- 이직 번호 - 하나의 효소가 초당 촉매 될 수있는 반응의 수
- 효소 - 아미노산으로 만든 생물학적 촉매.
- 잠금 및 키 모델- 효소와 반응물 분자가 반응의 특이성과 효율을 증가시키기 위해 활성 부위에서 유사한 형태를 갖는 모델. .
- 균질 촉매 - 반응물과 동일한 단계에 존재하는 촉매.
- 이종 촉매- 반응물과는 다른상에서 촉매.
우리는 이제 촉매가 무엇인지, 반응에 영향을 미치는지, 활성화 에너지가 어떻게 작동하는지 알기를 바랍니다. 화학 반응의 동역학을 더 깊이 파고 들면 이러한 개념이 더욱 중요해질 것입니다. Chemtalk를 방문해 주셔서 감사합니다!