핵심 개념
이 기사에서 우리는 효소 보조 인자의 세 가지 주요 그룹 인 메커니즘과 중요성을 탐구합니다 :금속 이온, 코비 스트레이트 및 보철 그룹.
보조 인자와의 효소 촉매
생물학적 시스템에서 효소의 중요성을 과장하기는 어렵습니다. 단백질 합성, DNA 복제 및 대사를 포함하여 세포에 의해 수행되는 거의 모든 기능은 효소에 의해 촉진 된 화학 반응에 의존한다. 효소가 없으면, 이러한 과정은 생명이 존재하기에 빠르거나 정확하게 발생할 수 없었습니다. 효소에 의해 제공되는 다양한 기능으로 인해 세포는 다양한 효소 구조와 기능을 요구합니다.
세포의 효소 배열의 기능을 증가시키기 위해, 많은 효소-촉매 경로는 비 단백질 성분의 존재에 의존한다. 생화학 자들은 이러한 성분들을 "보조 인자"라고 부릅니다. 여기에는 금속 이온과 "코엔자임"을 포함하여 코엔자임 및 보철물을 나타냅니다. 각 유형의 보조 인자는 반응을 화학적으로 변형시키는 데 도움이되며 대부분의 경우 대체 할 수없는 역할을하는 경향이 있습니다. 보조 인자에 의존하는 반응의 경우, 효소는 공동 인자의 존재없이 비활성“아포 엔 자임”을 렌더링 할 수 있습니다. 그들의 보조 인자와 접촉하면,이 효소 복합체는 완전히 활성화 된 "holoenzymes"가된다.
효소 보조 인자 :금속 이온
많은 효소는 그들의 활성 부위에서 각각의 화학 반응을 촉매하기 위해 금속 이온을 요구한다. 이 금속 이온은 종종 불안정한 하전 그룹을 안정화시키는 데 도움이되거나 산화 환원 반응에 참여합니다. 이들 금속은 효소 촉매에서 이러한 중요한 용도를 사용하기 때문에, 이들 금속의 특정 미량 금액은 많은 유기체의식이 요법의 중요한 부분을 형성한다. 또한, 특정 다른 금속은 효소 작용의 영향으로 인해 독성 효과를 가질 수 있습니다. 주목할만한 예에는 CD 및 HG가 포함되며, 이는 해당 양이온에 의존하는 효소에서 Zn을 대체 할 수 있습니다. 그러나 CD와 HG는 동일한 촉매 효과가 없으므로 기능 장애 효소와 그 이온을 섭취하는 유기체의 건강에 부정적인 영향을 미칩니다.
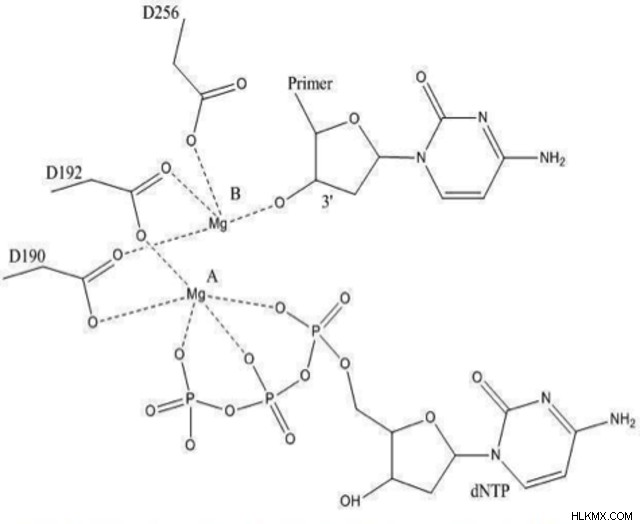
.아마도 효소-금속 관계의 가장 중요한 예는 DNA 폴리머 라제 및 Mg의 예를 포함한다. 구체적으로, DNA 폴리머 라제는 DNA 뉴클레오티드 사이의 포스 포디 에스테르 결합의 형성뿐만 아니라 가닥 사이의 염기 형 수소 결합을 촉진시킨다. 이를 효율적으로 수행하기 위해, 효소는 DNA 가닥의 골격을 형성하는 고도로 음전적으로 차지 된 인산염을 안정화시켜야한다. 마그네슘 양이온은 이들 그룹을 반대 전하로 안정화시켜 구조적 손상이나 가닥에 대한 연소없이 DNA 합성을 허용한다.
효소 보조 인자 :cosubstrates
금속 이온 외에도 효소는 또한 일부 유기 분자에 의존하여 기질 사이의 반응을 촉진하는 데 도움이 될 수 있습니다. 생화학 자들은“코엔자임”이라는 용어를 사용하여 이러한 유기 분자를 설명합니다. "코비 스트레이트"라고 불리는 특정 종류의 코엔자임은 효소에 화학적으로 부착되는 것이 아니라 효소 환경에 일시적으로 떠 다니는 것입니다. 또한, 다른 유형의 보조 인자와는 달리, 효소의 활성 부위에 대한 결합을 공제하고 기질과 함께 반응에 참여한다. 효소 촉매 작용은 코비 스트레이트를 "소비"합니다. 이는 Cosubstrate가 화학적으로 변형되고 추가 반응에 참여하기 위해 재생하기 위해 다른 반응에 참여해야 함을 의미합니다.
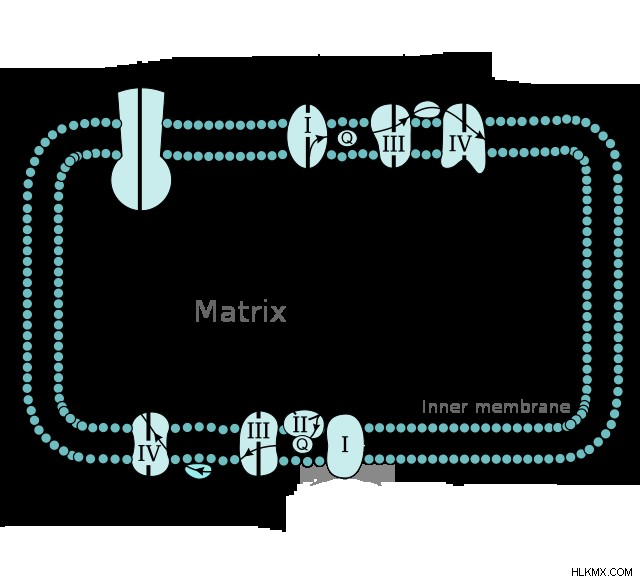
.니코틴 아미드 아데닌 디 뉴클레오티드 (NADH) 및 플라 빈 아데닌 디 뉴클레오티드 (FADH <서브> 2 )는 세포 호흡에 참여하기 때문에 진핵 생물 유기체에서 가장 중요한 코비 스트레이트 역할을합니다. 구체적으로, 당분 해 및 구연산 사이클에서, 그들의 산화 된 형태 (NAD 및 FAD)는 포도당을 화학적으로 변형함에 따라 효소에 의해 감소된다. 그런 다음 전자 수송 체인 동안 감소 된 코비 스트레이트 (NADH 및 FADH 2 ) 산화됩니다. 중요하게도, 이것은 산화 적 인산화를 통한 ATP의 합성에 힘을 발휘한다. 물론,이 새로 산화 된 형태는 추가 세포 호흡에 힘을 발휘할 수있다. NADH 및 FADH 2 활성화와 불 활성화가 효소 경로에서 목적을 달성하는 cosubstrates의 좋은 예입니다.
효소 보조 인자 :보철 그룹
또한 자유롭게 존재하기보다는 효소에 직접 부착하는 코엔자임이 존재한다. 생화학 자들은이 코엔자임을“보철기”라고 부르며 효소의 단백질과 강한 공유 결합을 갖는 경향이 있습니다. Cosubstrates와 마찬가지로, 보철 그룹은 재생이 촉매 적으로 활성화되기 위해 재생을 요구합니다. 그러나 Cosubstrates와 달리,이 재생은 다른 효소와 관련된 2 차 반응을 요구하기보다는 효소 반응 전체에서 발생합니다.
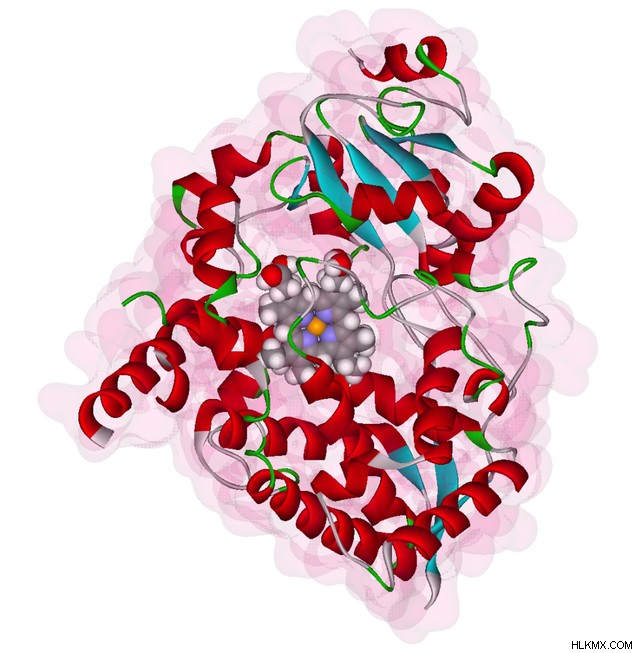
.중요한 보철의 한 예는 많은 다른 효소와 관련된 헴 그룹입니다. 구체적으로, 헴 그룹은 유기 구조에 내장 된 Fe 이온을 포함한다. 이 그룹은 중요한 산화 환원 반응을 촉진하는 데 도움이되므로 산화물이 산화제와 연관되는 경향이 있습니다. 또한, 헴 그룹은 헤모글로빈과 같은 비 효소 단백질에서 목적을 제공하며, 여기서 헴 그룹은 수송을 위해 산소에 결합한다.
.