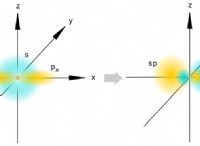
에탄의 탄소는 사면체 형상과 함께 배열 된 4 개의 결합을 포함한다. 더욱이, 탄소는 결합 길이가 1.54Å이고 각 탄소로부터 1 SP3 궤도의 겹침을 통해 이루어지는 반면, 6 개의 탄소 하이드로겐 결합은 2 개의 탄소에서 SP3의 남은 궤도와 수소 아톰의 1s 궤도에서 겹침으로 만들어진다. 그들은 두 개의 궤도의 엔드 앤 엔드 겹침으로 만들어지면서 자유롭게 회전하며 본질적으로 시그마 본드입니다.
에탄 분자의 경우, 이것은 두 개의 메틸, 즉 CH3 그룹이 허브에 두 바퀴로 묘사 될 수 있으며, 각각은 다른 사람과 관련하여 자유롭게 회전합니다.
.메탄의 탄소 원자와 마찬가지로 중심 질소는 암모니아에서 혼성화된다. 그러나 질소의 경우, 5 개의 원자가 전자가 설명되어 있으며, 이는 4 개의 하이브리드 궤도 중 3 개가 부분적으로 채워져 결합 할 수 있음을 의미합니다. 반면, 네 번째는 결합되지 않은 전자 쌍에 의해 완전히 점유된다.
더욱이, 에텐, 즉 C2H4 또는 에틸렌은 증기 균열 과정과 합성 적으로 제조 된 가스의 유형이다. 그것은 과일이 익을 수있는 신호를 제공하기 위해 식물에 의해 미량 금액으로 자연적으로 방출됩니다. 또한, 에텐은 2 개의 SP2 하이브리드 화 된 탄소 원자를 포함하고; 이들은 시그마 결합과 각각의 수소 원자로 서로 결합됩니다. 탄소상의 남은 비 브리드 화 된 p 궤도는 에텐에 반응성을 제공하는 PI 결합을 만듭니다.
에탄이란 무엇입니까?
그것은 본질적으로 유기적이며 화학적 공식을 갖는 화학 화합물입니다. C2H6. 에탄은 표준 온도에서 무색뿐만 아니라 무색입니다. 다른 많은 탄화수소와 마찬가지로, 에탄은 천연 가스와 석유 정제의 석유 화학 부산물 형태로 산업 규모로 분리됩니다.
주로 에틸렌 생산을위한 공급 원료로 사용됩니다. 또한, 관련 화합물은 수소 원자를 다른 기능 그룹으로 대체함으로써 결정될 수있다. 에탄 부분은 에틸기로 알려져있다. 예를 들어, 히드 록실 그룹과 연결된 에틸기는 음료에 존재하는 알코올 인 에탄올을 생성합니다.
에탄의 하이브리드 화
에탄은 일반적으로 2 개의 탄소 원자와 6 개의 수소 원자를 포함한다. 그러나, 탄소는 중심 원자로 남아 있으며, 그 궤도는 혼성화 과정에 관여합니다. PZ 궤도뿐만 아니라 C2H6, 1S 궤도 및 PX, PY의 제조 과정에서 SP3 하이브리드 화를 겪습니다. 이것은 각각의 탄소 원자에 대해 4 개의 하이브리드 화 된 궤도의 형성으로 이어진다.
그러나, 분자 하이브리드 궤도는 이제 전자 사이에 다른 결합을 생성한다. 4 개의 SP3 하이브리드 궤도로부터, 탄소 원자의 하나의 하이브리드 궤도는 3 개의 시그마 결합을 형성하기 위해 수소 원자의 하나의 S- 궤도와 겹친다. 또한, 마지막 궤도는 다른 탄소 원자의 하나의 SP3 궤도와 겹쳐서 두 개의 탄소 원자 사이에 시그마 결합을 만듭니다.
에탄의 표현
에탄은 탄소-탄소 결합을 갖는 가장 간단한 분자이다. 에탄, 즉 CH3CH3에서, 두 탄소는 SP3 하이브리드 화되어 있으며, 이는 둘 다 사면체 형상과 4 개의 결합을 포함한다는 것을 의미한다. 탄소 탄소의 SP3 궤도는 탄소-탄소 σ 결합을 만드는 두 번째 탄소 원자의 SP3 궤도와 엔드 투 엔드를 중첩시킨다.
이 궤도 중첩은 표기법의 사용으로 정의됩니다. SP3 (c) -sp3 (c). 모든 단일 남은 SP3 하이브리드 궤도 궤도 궤도는 탄소 배열 σ 결합을 만드는 수소 원자의 궤도와 겹칩니다.
σ 탄소-탄소 결합은 길이 154 pm의 결합뿐만 아니라 377 kJ/mol의 강도를 갖는 결합을 갖는다. 탄소-하이드로겐 σ 결합은 메탄보다 421 kJ/mol의 강도로 약간 약하다. 더욱이, 에탄의 C-C-H 결합 각도는 111.2도이며, 이것은 사면체 분자에 대해 예상되는 것에 가깝습니다.
명심해야 할 필수 요점
- C2H6 또는 CH3CH3, 1S 궤도 및 3P 궤도 :PX, PY 및 PZ는 혼성화 과정에 관여합니다.
- SP3 하이브리드 화 된 4 개의 궤도가 형성되어 있습니다.
- 에탄의 혼성화 당시, 완벽한 사면체 기하학으로 4 개의 유사한 결합이 생성됩니다.
결론
에탄에서, 단일 탄소 원자에 대해 4 개의 하이브리드 화 된 궤도가 생성된다. 또한, PX, PY 및 PZ Orbitals를 포함하여 C2H6, 1S 궤도의 제조 과정에서 SP3 혼성화를 겪는다. 이것은 각 탄소 원자에 대해 4 개의 하이브리드 화 된 궤도의 생성으로 이어진다. 기사 끝에 에탄 질문에 대한 혼성화가 있습니다.