질문에 대답하려는 시도에서 황산염 이온에 대한 테스트는 무엇입니까? ) 이온. 이러한 모든 시험 방법은 설페이트가 다른 화학 시약과 반응 할 수있게함으로써 시각적 관찰을 포함한다. 침전 방법은 황산염 이온의 분석에 널리 사용됩니다. 금속 침전물 중 일부는 INDROUS 염산 및 희석 질산에서 불용성과 같은 독특한 특성을 가지고; 탄산염, 인산염 및 설파이트의 것도 같은 방식으로 행동하지 않습니다. 이러한 방법은 황산염을 다른 사람과 구별하는 데 사용될 수 있습니다. 이러한 테스트 방법 중 일부는 매우 민감합니다. 소량으로 존재하더라도 식별 할 수 있습니다.
황산염 이온 테스트
물의 황산염 이온 테스트-물에서 금속 황산염의 용해도
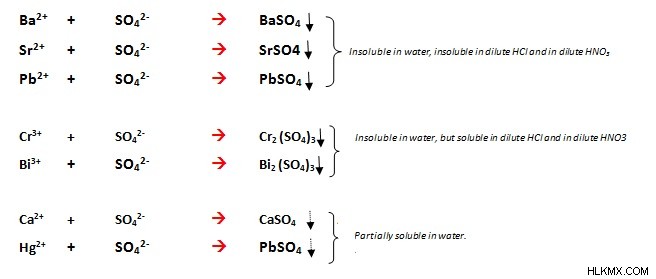
바륨 (BASO4), 스트론튬 (SRSO4) 및 납 (PDSO4)의 황산염은 물에 불용성이없고, 칼슘 (CASO4) 및 수은 (HGSO4)은 부분적으로 물에 적합합니다. 다른 금속 황산염의 대부분은 물에 용해됩니다. 수은, 비스무트 및 크롬과 같은 기본 황산염 중 일부는 물에 불용성이지만 그 황산염은 희석 된 질병 또는 염산에 용해됩니다.
황산염 이온에 대한 염화 바륨 검사
바륨 클로라이드 (bacl 2 )는 황산염 용액에 첨가되고, 흰색의 침전물이 형성된다. 따뜻한 희석 염산과 희석 질산에 불용성이지만 끓을 때 가용성이 있습니다.
ba 2 + + so 4 -> BASO4 ↓ (흰색)
이 테스트는 일반적으로 희석 된 염산을 추가하여 산성 매체에서 수행됩니다. 탄산염 (CO3), 황산염 (SO3) 및 인산염 (PO4) 은이 조건 하에서 침전되지 않습니다.
바륨 황산염에 대한 칼륨 과망간산염 테스트
바륨 황산염이 칼륨 과망간산산염 (KMNO4)의 존재하에 침전 된 경우, 일부 과망간산산염을 흡수 한 후 분홍색 (바이올렛) 색상으로 변합니다. 표면의 흡착 된 과망간산산염은 일반적인 환원제를 사용하여 감소 될 수 없습니다. 과산화수소조차도 감소를위한 효과적인 시약이 아닙니다. 표면에 흡착되지 않은 과도한 칼륨 과망간산염은 일반적인 환원제와 쉽게 반응합니다. 따라서 분홍색 바륨 황산염은 무색 매체에서 명확하게 보입니다.
황산염 이온에 대한 아세테이트 테스트
납 아세테이트가 설페이트 용액에 첨가되면 황산 납의 백색 침전물이 형성됩니다. 그것은 뜨거운 농축 황산, 암모늄 아세테이트 용액 및 수산화물 용액에 용해됩니다.
pb + so4-> pbso4 ↓ (흰색)
마지막 경우 (naOH를 사용한 pbso4)에서, 나트륨 테트라 하이드 록스 소아미네이트 (II)가 형성됩니다. 염산으로 산성화 된 염화 염화 납은 배지에서 결정화됩니다.
pbso4 ↓ + naoh-> na 2 [PB (OH) 4 ] + SO4
황산염 이온에 대한은 질산염 테스트
은 질산은이 황산염 용액에 첨가되면은 황산염의 결정질 침전물이 형성됩니다. 이것은 농축 용액 (Ag 2 의 용해도에서만 발생합니다 그래서
ag + so4-> ag 2 SO4 ↓
황산염 이온에 대한 수은 질산염 테스트
수은 질산염이 설페이트 이온 용액에 첨가 될 때, 기본 수은 황산염 (HGSO4)의 황색 침전물이 형성됩니다.
3Hg + SO4 + 2H 2 O -> 4H+ HGSO4.2HGO ↓ (노란색)
이것은 민감한 테스트이며 바륨 또는 납 황산 납의 현탁액에서도 관찰 할 수 있습니다.
황산염 테스트 - 요약
설페이트는 독특한 용해도 특성을 가진 일부 금속 이온과 침전됩니다. 그것은 모든 금속 이온과 함께 침전물을 형성하지는 않지만 바륨, 스트론튬 및 납 (Baso4, SRSO4, PBSO4)을 사용하면 물 불용성 침전물을 형성합니다. 그들은 따뜻한 희석 염산 또는 질산에 용해되지 않지만 온난화시 용해됩니다. 일부 황산염 (bi 2 (SO4) 3, CR2 (SO4) 3)는 물에 불용성이지만 희석 된 HCl 및 희석 된 HNO3 산에 용해됩니다. 일부 황산염 (HGSO4, CASO4)은 부분적으로 물에 가용성이 있습니다. 수은 질산염은 황산염 이온의 존재 하에서 황색 침전을 제공하고; 이것은 농도가 상당히 낮더라도 식별하는 데 사용할 수 있습니다. 염화 바륨은 칼륨 과자 가산산염이 반응 배지에있을 때 황산염으로 분홍색 침전물을 형성합니다.