주요 차이-원자 대 분자
원자는 분자의 빌딩 블록입니다. 우리 주변의 모든 것은 분자 나 원자로 구성됩니다. 이 기사에서는 화학 물질과 물리적 특성과 관련하여 원자와 분자의 차이에 대해 논의 할 것입니다. 원자와 분자의 주요 차이점은 크기입니다. 원자는 원소의 가장 작은 성분 인 반면 분자는 둘 이상의 원자로 만들어집니다.
이 기사는
를 탐구합니다 1. 원자는 무엇입니까
- 정의, 구조, 속성
2. 분자는 무엇입니까
- 정의, 구조, 이온 결합, 공유 결합
3. 원자와 분자의 차이점은 무엇입니까? 
원자가 무엇입니까
원자는 요소의 가장 작은 구성 요소로 정의되며 특정 요소와 관련된 화학적 특성을 보여줍니다. 원자는 더 많은 양성자, 중성자 및 전자로 분해 될 수있다; 그러나,이 하위 원자 입자는 분리 될 때 원소의 화학적 특성을 나타내지 않는다. 특정 요소의 원자는 대부분 고정 된 수의 전자, 양성자 및 중성자를 포함합니다.
탄소 원자에는 6 개의 양성자, 6 개의 전자 및 6 개의 중성자가 포함되어 있습니다. 이러한 아 원자 입자의 이러한 조합은 C에 고유합니다. 그러나 일부 원소에는 동위 원소가 있습니다. 탄소는 그러한 요소 중 하나입니다. 동위 원소는 중성자 수가 다릅니다. 이것은 방사능을 일으킨다.
원자의 질량은 주로 양성자와 중성자에 의해 결정됩니다. 양성자는 양전하를 갖는 반면 전자와 중성자는 각각 음성 및 중성 전하를 갖는다. 원자의 핵은 유사한 전하의 반발력을 극복하기 위해 중성 중성자에 의해 서로 마련 된 양성자로 구성된다. 전자는 핵을 둘러싼 궤도라고 불리는 경로에서 무작위로 발견 될 수 있습니다.
원자는 화학 반응에 의해 아 원자 입자로 분리 될 수 없지만 핵 반응에 의해 분리가 가능합니다.
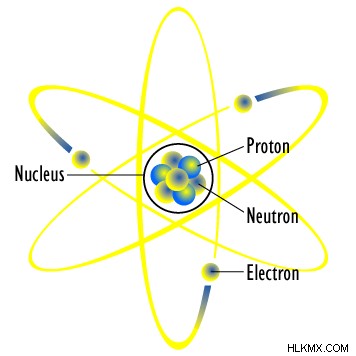
그림 1 :원자 구조
분자는 무엇입니까
분자는 전자 나 교환 전자를 공유하기 위해 함께 모이는 둘 이상의 원자로 만들어집니다. 분자의 이러한 원자는 다른 유형의 결합에 의해 함께 유지됩니다. 원자의 외부 껍질에있는 전자 만 본딩에 관여합니다.
이온 결합
전자는 원자들 사이에서 교환됩니다. 전자를 방출하는 원자는 양전하를 얻는 반면 전자를 얻는 원자는 음으로 하전됩니다. 이 반대로 하전 된 이온들 사이의 매력을 이온 결합이라고합니다.
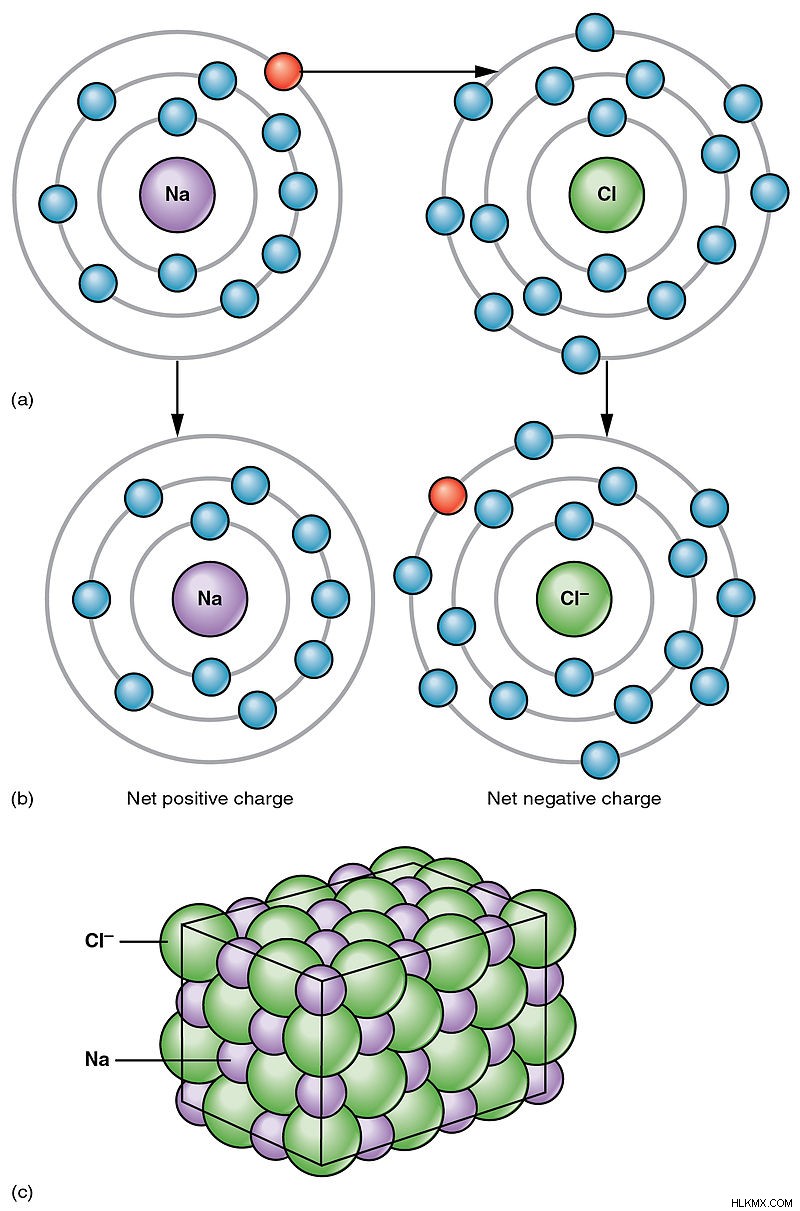
그림 2 :이온 결합의 예
클로라이드 나트륨의 예는 Na로부터의 하나의 전자가 Cl로 전달되어 Na에 양전하를 남긴다는 것을 보여준다. CL은 부정적인 충전이된다. 이 두 가지 반대로 하전 된 이온 사이의 매력으로 인해 NaCl은 이온 성 염으로 간주됩니다.
공유 결합
공유 결합은 두 원자 사이에 전자를 공유하여 형성됩니다. 따라서, 공유 전자 쌍은 관련된 원자에 속한다. 공유 결합은 단일 결합뿐만 아니라 이중 및 삼중 채권과 같은 다수의 결합을 일으킬 수있다. (읽기 : 공유 결합은 어떻게 형성됩니까 )
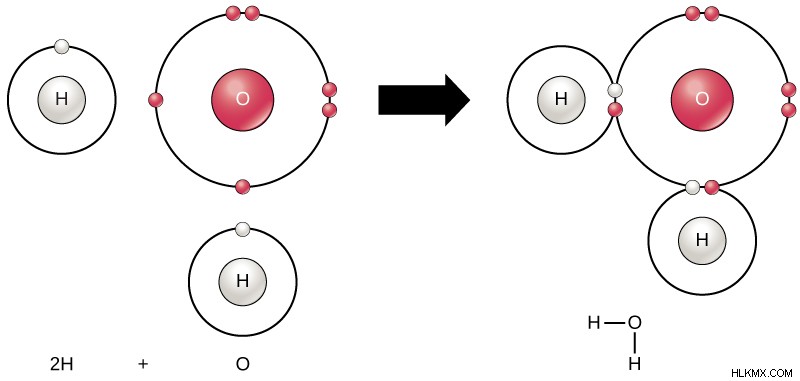
그림 3 :공유 결합의 예
더 읽기 :공유 결합과 이온 결합의 차이
원자와 분자의 차이
원자 : 원자는 분자의 빌딩 블록입니다. 해당 요소의 화학적 특성을 표시하는 가장 작은 단수체.
분자 : 분자는 둘 이상의 원소로 만들어집니다. 그들은 구성 요소의 개별 속성을 표시하지 않습니다.
구성 요소
원자 : 원자는 아 원자 입자로 구성됩니다 :양성자, 전자, 중성자.
분자 : 분자는 동일한 요소 또는 다른 원소 일 수있는 두 개 이상의 원자로 구성됩니다.
안정성
원자 : 원자는 단독으로 안정적이지 않으며 다른 원자와 화학적 결합을 만들어 안정이됩니다.
분자 : 분자는 단독으로 안정적입니다.
분리
원자 : 원자는 화학 반응에 의해 아 원자 입자로 분리 될 수 없다. 분리는 원자력에 의해서만 가능합니다.
분자 : 분자는 화학 반응에 의해 원자로 분리 될 수있다.
결론
원자와 분자는 우주의 창립 엔티티입니다. 앞에서 논의한 바와 같이, 원자는 분자를 구성합니다. 그러나, 원자의 화학적 특성은 분자를 형성 할 때 종종 유지되지 않습니다. 예를 들어, Na는 반응성이 높은 금속이고 Cl은 독성 가스입니다. 그러나, 테이블 소금 (NaCl)은 금속이나 독성이 아닙니다. 이것은 원자의 화학적 특성이 분자가 될 때 변화되었음을 나타냅니다.
분자는 화학적 수단에 의해 구성 원자로 분리 될 수 있습니다. 이것은 원자에서는 불가능합니다. 원자는 핵 반응에 의해 아 원자 입자로 분리 될 수있다.
분자는 자체적으로 존재할 수 있으며 종종 안정적입니다. 그러나 이것은 원자의 경우가 아닙니다. 고귀한 가스 구성이있는 원자 만 자체적으로 안정적 일 수 있습니다. 아르곤, 헬륨, 크립톤 등은 이러한 원자의 일부 예입니다. 안정성의 이유는 외부 껍질의 최대 전자 수에 도달했기 때문입니다. 따라서 청구가 표시되지 않습니다. 그러나 이런 종류의 안정성이없는 원자는 분자를 만들고 안정된 전자를 공유하거나 전달하는 데 함께 모입니다.