주요 차이 - 알칼리 금속 대 알칼리성 지구 금속
지구의 모든 요소는 금속, 비 메탈, 메탈 로이드 및 불활성 가스로 분류 할 수 있습니다. 비활성 가스는 안정적인 외부 옥트의 존재로 인해 반응성이 제로가있는 원소입니다. 메탈 로이드는 금속과 비 메탈의 특정 특성을 가진 요소입니다. 비금속은 금속의 속성을 가지고 있지 않은 요소입니다. 금속은 우수한 전기 및 열전도율, 광택을 포함하여 고유 한 특성 세트를 갖는 요소입니다. 금속은주기 테이블의 왼쪽과 중간 부분에 배치됩니다. 주기적인 테이블의 모든 금속은 세 그룹, 즉 세 그룹으로 분류됩니다. 알칼리 금속, 알칼리성 지구 금속 및 전이 금속. 알칼리 금속과 알칼리성 지구 금속의 주요 차이점은 알칼리 금속이 가장 바깥 쪽 궤도에 하나의 원자가 전자를 가지고 있다는 것입니다 알칼리성 지구 금속은 가장 바깥 쪽 궤도에 2 개의 원자가 전자가 있습니다.
이 기사에서
를 검사합니다 1. 알칼리 금속은 무엇입니까
- 정의, 특성, 속성, 예
2. 알칼리성 지구 금속은 무엇입니까
- 정의, 특성, 속성, 예
3. 알칼리 금속과 알칼리성 지구 금속의 차이점은 무엇입니까

알칼리 금속
알칼리 금속은 가장 바깥 쪽 쉘에 하나의 원자가 전자 만있는 요소입니다. 이 금속은 주기율표의 그룹 IA에 배치됩니다. 이 금속에는 리튬, 나트륨, 칼륨, 루비듐, 세슘 및 프란치움이 포함됩니다. 가장 바깥 쪽 쉘에 단일 전자를 전자-수용 원자에 기증함으로써, 이들 금속은 양으로 하전되어 고귀한 가스의 전자 구성을 얻습니다. 모든 알칼리 금속은 이온 성이며 전기성을 나타냅니다. 양으로 하전 된 핵은 전자가 채워진 내부 쉘의 존재로 인해 가장 바깥 쪽 전자에 대한 인력이 적기 때문에 전자-전달 경향은 그룹 아래로 증가한다. 다른 금속의 대부분과 달리 알칼리 금속은 저밀도와 낮은 융점으로 부드럽습니다. 이 금속은 주기율표의 모든 금속 중에서 가장 반응합니다.
알칼리성 지구 금속
알칼리성 지구 금속은 가장 바깥 쪽 쉘에 두 개의 원자가 전자가있는 금속입니다. 베릴륨, 마그네슘, 칼슘, 스트론튬, 바륨 및 라듐을 포함한 6 개의 알칼리성 지구 금속이 있습니다. 그들은 가장 바깥 전자의 기증을 통해 고귀한 가스의 전자 구성을 얻음으로써 안정적이됩니다. 전자가 전기 음성 원자로 주어지면 알칼리성 지구 금속이 긍정적으로 하전됩니다. 알칼리성 지구 금속은 반응성이 높은 금속이며 주기율표의 두 번째 열에 배치됩니다. 이 금속은 세계의 모든 것을위한 빌딩 블록입니다. 이 금속은 종종 자연의 설페이트 형태로 발견됩니다. 예제는 석고와 같은 미네랄; 황산 칼슘, Epsomite; 황산 마그네슘 및 바라이트; 황산 바륨.
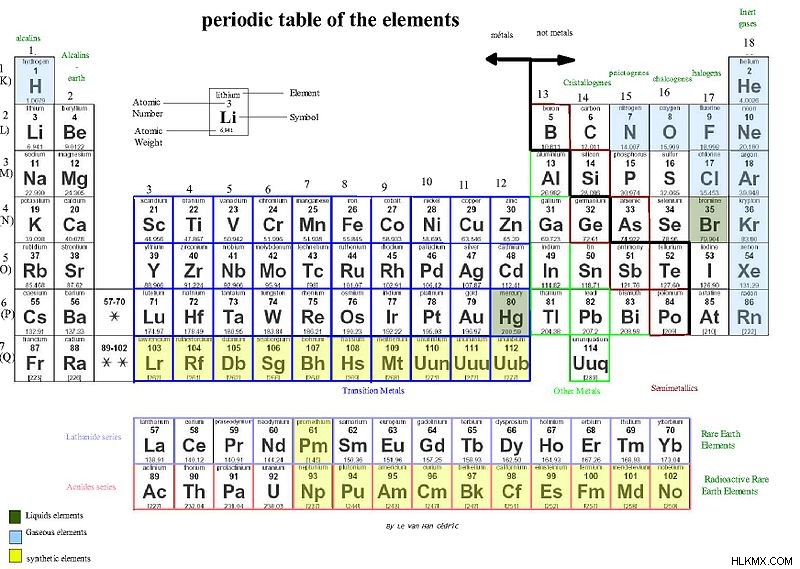
그림 1 :알칼리 및 알칼리성 지구 금속을 보여주는주기 테이블
알칼리 금속과 알칼리성 지구 금속의 차이
원자의 가장 바깥 쪽 쉘에있는 전자 수
알칼리 금속 : 각 알칼리 금속에는 단일 전자가 있습니다.
알칼리성 지구 금속 : 각 알칼리성 지구 금속에는 두 개의 전자가 있습니다.
금속의 특성
알칼리 금속 : 알칼리 금속은 부드럽습니다.
알칼리성 지구 금속 : 알칼리성 지구 금속은 단단합니다.
용융점
알칼리 금속 : 알칼리 금속은 녹는 점이 낮습니다.
알칼리성 지구 금속 : 알칼리성 금속은 비교적 융점이 비교적 높습니다.
금속 수산화물의 특성
알칼리 금속 : 알칼리 금속의 수산화물은 매우 기본적입니다.
알칼리성 지구 금속 : 알칼리성 지구 금속의 수산화물은 비교적 덜 기본적입니다.
탄산염 분해
알칼리 금속 : 알칼리 금속의 탄산염은 분해되지 않습니다.
알칼리성 지구 금속 : 알칼리성 지구 금속의 탄산염은 고온으로 가열 될 때 산화물을 형성하도록 분해됩니다.
질산염 가열
알칼리 금속 : 알칼리 금속의 질산염은 해당 질산염과 산소를 제품으로 제공합니다.
알칼리성 지구 금속 : 알칼리성 지구 금속의 질산염은 상응하는 산화물, 이산화 질소 및 산소를 제품으로 제공합니다.
가열에서 수산화물의 안정성
알칼리 금속 : 알칼리 금속의 수산화물이 안정적입니다.
알칼리성 지구 금속 : 알칼리성 지구 금속의 수산화물 산화물을 형성합니다.
실온에서 중탄산염의 특성
알칼리 금속 : 알칼리 금속의 중탄산염은 견고한 형태로 존재합니다.
알칼리성 지구 금속 : 알칼리성 지구 금속의 중탄산염은 용액 형태로 존재합니다.
가열시 퍼 옥사이드의형성
알칼리 금속 : 알칼리 금속은 가열 될 때 과산화물을 형성합니다.
알칼리성 지구 금속 : 바륨을 제외한 알칼리성 지구 금속은 과산화물을 형성하지 않습니다.
질화물 형성
알칼리 금속 : 알칼리 금속은 리튬을 제외하고는 질화물을 형성하지 않습니다.
알칼리성 지구 금속 : 알칼리성 지구 금속은 안정적인 질화물을 형성합니다.
탄화물 형성
알칼리 금속 : 알칼리 금속은 리튬을 제외하고 탄화물을 형성하지 않습니다.
알칼리성 지구 금속 : 알칼리성 지구 금속은 안정적인 탄화물을 형성합니다.
예제
알칼리 금속 : 리튬, 나트륨, 칼륨, 루비듐, 세슘 및 프란치움은 알칼리 방법의 예입니다.
알칼리성 지구 금속 : 베릴륨, 마그네슘, 칼슘, 스트론튬, 바륨 및 라듐은 알칼리성 지구 금속의 예입니다.
요약
알칼리 금속 및 알칼리성 지구 금속은 원자의 가장 바깥 쪽 쉘에 각각 단일 및 이중 원자가 전자를 포함하는 중요한 요소입니다. 알칼리 금속과 알칼리성 지구 금속의 주요 차이점은 원자의 가장 바깥 쪽 껍질에있는 전자의 수와 그 후 주기율표에서의 위치입니다. 알칼리 금속 (리튬, 나트륨, 칼륨, 루비듐, 세슘 및 프랑크)은 첫 번째 컬럼 (IA)에 배치되는 반면, 알칼리성 지구 금속 (베릴륨, 마그네슘, 칼슘, 스트론륨, 바륨 및 라듐)은 주기적 테이블의 두 번째 컬럼 (IA)에 배치됩니다. 두 금속 그룹은 모두 반응성이 높습니다. 금속이 불꽃 위로 가열 될 때이 금속이 독특한 화염 색상을 나타내므로 화염 테스트를 사용하여 이러한 금속을 모두 식별 할 수 있습니다.
. 참조 :
1. Trefil, J. S. (2001). 과학 기술 백과 사전 . Taylor &Francis.
2. Bridget Heos (2010). 알칼리성 지구 금속 :베릴륨, 마그네슘, 칼슘, 스트론튬, 바륨, 라듐, 뉴욕 :Rosen Central.
3. Raymond Fernandes (2008). 클래스 10의 살아있는 과학 화학, Ratna Sagar P. Ltd.
이미지 제공 :
1. "요소의 주기성 테이블"Le van Han Cédric-levanhan (gfdl)을 통해 커먼즈 위키 미디어