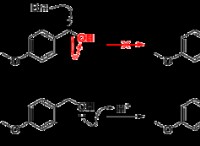
대조적으로, 이온 성 화합물은 서로 밀접하게 끌리는 양의 및 음으로 하전 된 이온으로 구성됩니다. 이온 성 화합물을 용해시키기 위해, 용매 분자는 이러한 강력한 이온 인물을 극복하고 이온을 둘러싸고 안정적인 용 매화 구체를 형성 할 수 있어야한다. 휘발유와 같은 비극성 용매는 하전 입자와 잘 상호 작용하지 않기 때문에이를 수행 할 능력이 없습니다.
결과적으로, 이온 성 화합물은 전형적으로 유전 상수가 높고 이온을 효과적으로 용매 할 수있는 물과 같은 극성 용매에만 용해됩니다.