리튬 (Li) 및 염소 (CL) 원자가 상호 작용하여 이온 결합을 형성 할 때, 이들의 원자가 전자는 안정적인 전자 구성을 달성하기 위해 재 배열을 겪는다. 다음은 다음과 같습니다.
1. 초기 전자 구성 :
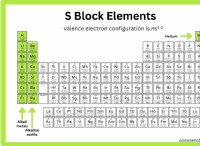
- 리튬 (Li) :1S²2S¹ (3 개의 원자가 전자)
- 염소 (CL) :1S²2S²2P⁶3S²3P⁵ (7 개의 원자가 전자)
2. 전자 전달 :
- 리튬은 하나의 원자가 전자를 염소로 전달합니다.
- 염소는이 전자를 받아들이고 음으로 하전됩니다.
- 결과적으로 리튬은 전자를 잃고 양으로 하전되며 염소는 전자를 얻고 음으로 하전됩니다.
3. 이온의 형성 :
- 리튬 원자는 유일한 원자가 전자를 잃어 1s² 전자 구성으로 양으로 하전 된 리튬 이온 (LIA)을 초래합니다.
- 염소 원자는 여분의 전자를 얻어 1S²2S²2P⁶3S²3P⁶ 전자 구성으로 음으로 하전 된 클로라이드 이온 (CL⁻)을 초래합니다.
4. 이온 결합 형성 :
- 양으로 하전 된 리튬 이온 (li⁺)과 음으로 하전 된 클로라이드 이온 (Cll) 사이의 정전기 인력은 이온 결합을 형성합니다.
요약하면, 리튬과 염소 사이의 이온 성 결합의 형성은 리튬에서 염소로의 하나의 원자가 전자를 전달하여 양으로 하전 된 리튬 이온 (li⁺) 및 음의 하전 클로라이드 이온 (CL)의 형성을 초래한다. 그런 다음 이들 이온은 반대 전하 사이의 강력한 정전기력에 의해 함께 유지되어 이온 성 화합물 클로라이드 (LICL)를 형성한다.