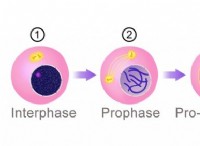
다음은 고장입니다.
* 파동 입자 이중성 : 전자는 파동 및 입자 특성을 모두 나타낸다. 그들의 파동 특성은 파동 함수로 설명되며, 이는 특정 위치에서 전자를 찾을 확률을 지시합니다.
* 확률 분포 : 전자 궤도는 전자를 찾을 확률이 높은 영역을 나타냅니다. 견고하고 정의 된 경계가 아닙니다.
* 모양과 에너지 : 궤도에는 뚜렷한 모양 (S, P, D, F)과 에너지 수준이 있습니다. 모양은 우주에서 전자 파동 함수의 분포를 반영하고 에너지 수준은 에너지를 결정합니다.
* 양자 수 : 각 궤도는 4 개의 양자 번호 세트 (n, l, m l 로 정의됩니다. , m s ) 전자의 에너지, 모양, 공간 방향 및 스핀을 설명합니다.
본질적으로, 전자 궤도는 우리가 움직임을 정확하게 추적 할 수는 없지만 원자 내의 전자의 거동을 이해하는 데 도움이되는 모델입니다.
여기에 비유가 있습니다. 깜박 거리는 전구가 있다고 상상해보십시오. 빛의 입자 (광자) 자체를 볼 수는 없지만 빛의 강도와 조명 영역을 관찰 할 수 있습니다. 마찬가지로, 우리는 전자를 볼 수 없지만 궤도를 사용하여 가능한 위치와 에너지 수준을 이해할 수 있습니다.