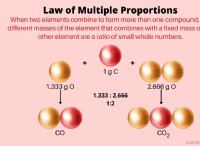
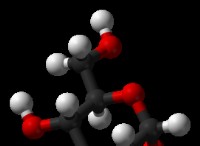
* 화합물 : 이들은 둘 이상의 원소가 고정 비율로 화학적으로 결합 될 때 형성된 물질이다. 예로는 물 (H (O), 소금 (NaCl) 및 설탕 (C₁₂H₂₂o₁₁)이 있습니다.
* 혼합물 : 이들은 둘 이상의 물질이 물리적으로 결합되지만 화학 반응을 겪지 않을 때 형성됩니다. 물질은 개별 특성을 유지합니다.
화합물의 혼합물의 예 :
* 바닷물 : 소금 (NaCl)과 물 (HATER)의 혼합물.
* 공기 : 질소 (NIT), 산소 (OAT), 이산화탄소 (COS) 등을 포함한 다양한 가스의 혼합물.
* 모래와 설탕 : 2 개의 고체 화합물의 혼합물.
* 커피 : 커피 땅 (다양한 화합물)과 물의 혼합물.
혼합물과 화합물의 주요 차이점 :
* 화학 결합 : 화합물은 화학적 결합을 통해 형성되는 반면, 혼합물은 그렇지 않습니다.
* 고정 비율 : 화합물은 고정 비율의 원소를 가지며, 혼합물은 가변 비율을 가질 수 있습니다.
* 분리 : 혼합물의 성분은 물리적 수단 (예 :여과, 증발)에 의해 분리 될 수 있으며, 화합물을 분리하려면 화학 반응이 필요합니다.
요약 : 혼합물은 다른 화합물을 결합하여 형성 될 수 있으며, 이러한 혼합물은 일상 생활의 어느 곳에서나 발견됩니다.