1. 균형 화학 방정식을 작성하십시오 :
* 반응의 반응물 및 생성물을 식별하십시오.
* 화학량 론적 계수를 조정하여 방정식의 균형을 유지하십시오.
2. 가능한 제품을 결정하십시오 :
* 잠재적 제품의 용해도를 예측하려면 용해도 규칙을 사용하십시오.
* 용해도 규칙 :
* 일반적으로 가용성 :
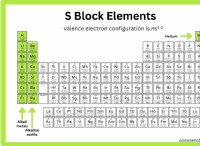
* 그룹 1 (Li, NA, K, RB, CS) 양이온
* 그룹 2 (CA, SR, BA) 양이온
* 암모늄 (NH4+) 양이온
* Ag+, pb2+, Hg2^2+를 제외하고 할로겐 (CL, BR, i)
* SR2+, BA2+, PB2+, CA2+를 제외한 황산염 (SO4^2-) (약간 가용성)
* 일반적으로 불용성 :
* 탄산염 (CO3^2-)
* 인산염 (po4^3-)
* 수산화물 (OH-)
* 황화물 (s^2-)
* 산화물 (O^2-)
* 예외 :
* 규칙에는 항상 예외가 있으므로 확인을 위해 용해도 차트를 참조해야 할 수도 있습니다.
3. 침전물을 식별하십시오 :
* 잠재적 제품 중 하나 또는 둘 다 용해도 규칙에 따라 불용성이라면 솔루션에서 고체로 침전 될 것입니다.
4. 순 이온 방정식 (선택 사항)을 작성하십시오.
* 순 이온 방정식은 관중 이온을 제외하고 반응에 참여하는 이온만을 보여줍니다.
예 :
반응 : 납 (II) 질산염 (AQ) + 요오드화 칼륨 (AQ) →
1. 균형 방정식 :
* PB (NO3) 2 (AQ) + 2KI (AQ) → PBI2 (S) + 2KNO3 (AQ)
2. 가능한 제품 :
* PBI2 (LEAD (II) 요오드 라이드)
* KNO3 (질산 칼륨)
3. 침전물 :
* PBI2는 용해도 규칙에 따라 불용성입니다 (Halides는 일반적으로 가용성이지만 리드는 예외입니다).
4. 순 이온 방정식 :
* pb^2 + (aq) + 2- (aq) → PBI2 (S)
따라서, 황색 침전물 (PBI2)의 형성은 이중 대체 반응이 발생했음을 나타냅니다.