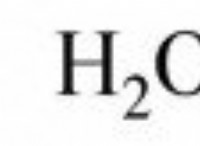기본 이해 :
* 양성자 및 중성자 : 산소는 핵에 8 개의 양성자와 8 개의 중성자가 있습니다.
* 전자 : 산소에는 핵을 공전하는 8 개의 전자가 있습니다.
* 에너지 레벨 (껍질) : 전자는 껍질이라고 불리는 특정 에너지 수준을 차지합니다. 첫 번째 쉘은 최대 2 개의 전자를 유지할 수 있고, 두 번째 쉘은 최대 8 개의 전자를 유지할 수 있습니다.
다이어그램 그리기 :
1. 핵 : 산소 원자의 핵을 나타 내기 위해 큰 원을 그립니다. 원 안에 "8p+"(8 개의 양성자)와 "8n"(8 중성자)을 씁니다.
2. 첫 번째 쉘 : 첫 번째 에너지 레벨 (쉘)을 나타 내기 위해 핵 주위에 작은 원을 그립니다. 이 원 안에 2 개의 점 (전자 표현)을 놓습니다.
3. 두 번째 쉘 : 두 번째 에너지 레벨을 나타내는 첫 번째 쉘 주위에 더 큰 원을 그립니다. 이 원 안에 6 개의 점 (전자)을 놓습니다.
완성 된 다이어그램 :
```
2E-의 뜻
-----
/ \ \
8p+ 8n 6e-
\ _____/
```
키 포인트 :
* Bohr-Rutherford 모델은 원자 구조의 단순화 된 표현입니다.
* 전자는 실제로 다이어그램에서 알 수 있듯이 깔끔한 원으로 핵을 공전하지 않습니다.
*이 모델은 전자의 배열을 시각화하고 기본 원자 특성을 이해하는 데 유용합니다.