그들이하는 방법은 다음과 같습니다.
* 활성화 에너지 : 모든 화학 반응은 활성화 에너지라고 불리는 일정량의 에너지가 필요합니다. 이 에너지는 분자가 움직이고 반응하는 "푸시"와 같습니다.
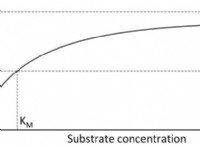
* 촉매로서의 효소 : 효소는 생물학적 촉매로서 작용한다 . 그들은 그 과정에서 소비하지 않고 반응을 가속화합니다. 그들은 낮은 활성화 에너지 로 대안적인 반응 경로를 제공함으로써이를 수행합니다. .
* 효소가 활성화 에너지를 낮추는 방법 : 효소는 기질이라 불리는 특정 분자에 결합한다. 이 바인딩은 임시 단지를 만듭니다.
* 오리엔트 반응을 선호하는 방식으로 기질.
* 균주 기판의 결합으로 인해 깨지기가 더 쉬워집니다.
* 는 대체 반응 환경을 제공합니다 그것은 에너지 장벽을 낮추게합니다.
이렇게 생각하십시오 : 언덕 위로 바위를 밀어야한다고 상상해보십시오. 언덕은 활성화 에너지를 나타냅니다. 효소는 언덕 위로 올라가는 것을 건설하는 것과 같습니다. 경사로는 바위를 반대편으로 데려 오는 데 적은 노력이 필요합니다.
활성화 에너지를 낮추면 효소가 반응이 훨씬 빨리 발생하여 삶의 필수 과정을 가능하게합니다.