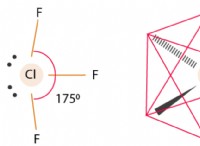
* 구리의 특성 : 구리는 상대적으로 반응하지 않는 금속이므로 전자를 쉽게 포기하지 않습니다. 그러나 강한 산화제에 의해 산화 될 수 있습니다.
* 질산의 특성 : 질산은 강한 산화제입니다. 전자를 쉽게 받아들이는 질산염 이온 (NOI)을 포함합니다.
* 반응 : 구리가 질산과 반응 할 때, 질산 질산 이온 (NOI)은 질산이 구리 원자를 산화시켜 전자를 멀리 잡아 당깁니다. 이는 구리 이온 (Cu²⁺)의 형성을 초래한다. 질산염 이온은 과정에서 질소 산화물 (NOI 또는 NO)으로 감소된다.
여기 단순화 된 화학 방정식이 있습니다 :
Cu + 4hnohn → Cu (No₃) ₂ + 2no₂ + 2h₂o
키 포인트 :
* 산화 : 구리는 산화되어 전자를 잃고 구리 이온이됩니다.
* 감소 : 질산염 이온이 감소하여 전자를 얻고 산화 질소가됩니다.
* 질산 구리의 형성 : 구리 이온은 질산염 이온과 조합하여 가용성 화합물 인 질산 구리 (Cu (NOI) ₂)를 형성한다.
* 적신 가스 : 생산 된 이산화 질소 (NOI) 가스는 반응에서 종종 관찰되는 적갈색의 색상입니다.
중요한 참고 : 구리와 질산 사이의 반응은 많은 금속의 염산과 같은 다른 산과의 반응과 달리 수소 가스 (H₂)를 생성하지 않습니다. 질산은 수소의 형성을 방지하기에 충분한 산화제이기 때문입니다.