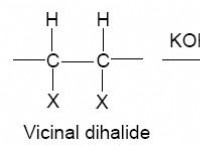
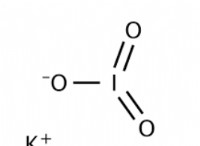
* 많은 조합 : 탄소와 수소는 다양한 비율로 결합하여 수많은 화합물을 형성 할 수 있습니다. 가장 일반적인 예는 다음과 같습니다.
* 알칸 : 일반식 CNH2N+2 (예 :메탄 -C4, 에탄 -C2H6, 프로판 -C3H8)
* Alkenes : 일반적인 공식 CNH2N (예 :Ethene -C2H4, 프로펜 -C3H6)
* alkynes : 일반 공식 CNH2N -2 (예 :Ethyne -C2H2, Propyne -C3H4)
* 주기적 탄화수소 : 이들은 사이클로 알칸, 사이클로 알켄 및 벤젠과 같은 방향족 탄화수소를 포함하여 다양한 구조와 공식을 갖는다 (C6H6).
* 이성질체 : 동일한 공식을 사용하더라도 원자 (이성질체)의 다른 배열이 존재할 수있어 다른 화합물을 초래할 수 있습니다. 예를 들어, 부탄 (C4H10)의 2 개의 이성질체 :N- 부탄 및 이소 부탄이 있습니다.
요약 :
특정 탄소 수 소화물에 대해 논의하려면 탄소 및 수소 원자의 수와 그 배열을 고려하여 특정 화합물을 이름 또는 화학 공식으로 지정해야합니다.