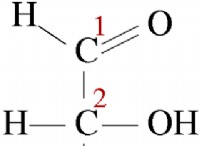
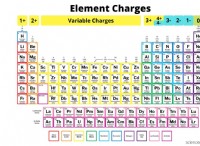
* 산화 수가 할당됩니다 : 그것들은 요소의 고유 한 속성이 아닙니다. 우리는 화학 결합에서 전자를 공유하거나 전달되는 방법을 이해하는 데 도움이되는 일련의 규칙에 따라 산화 번호를 할당합니다.
* 산화 수는 양수 또는 음수 일 수 있습니다 : 그들은 화합물에서 원자 경험을 산화 정도 (전자 손실) 또는 감소 (전자의 이득)를 나타냅니다.
* 산화 수는 화합물에 의존한다 : 동일한 원소는 다른 화합물에서 다른 산화 수를 가질 수 있습니다. 예를 들어, 염소는 NaCl에서 -1, HCLO +1, CLO4- +7의 산화 수를 가질 수 있습니다.
따라서 요소에 대해 가능한 가장 큰 산화 수는 특정 화합물에 따라 다릅니다.
그러나 몇 가지 일반적인 추세가 있습니다.
* 비금속 : 비금속은 전자를 더 쉽게 얻을 수 있기 때문에 최대 산화 수가 더 높은 경향이 있습니다. 예를 들어, 염소는 과염소산염 (CLO4-)에서 +7 산화 상태에 도달 할 수 있습니다.
* 금속 : 금속은 일반적으로 최대 산화 수가 더 낮습니다. 그들은 전자를 잃고 산화 상태가 양성인 경향이 있습니다.
요약하면, 산화 수가 가장 큰 단일 요소는 없습니다. 특정 화학 환경에 따라 다릅니다.