다음은 고장입니다.
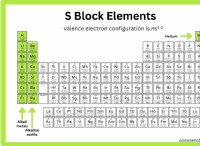
* 안정적인 전자 구성 : 원자는 가장 바깥 쪽 전자 쉘 (원자가 쉘)이 채워질 때 가장 안정적입니다. 대부분의 원자의 경우, 이는 원자가 쉘에 8 개의 전자를 갖는 것을 의미합니다 (Octet Rule).
* 공유 전자 : 자체적으로 안정적인 옥셋을 달성하기에 충분한 원자가 전자가없는 원자는 다른 원자와 전자를 공유 할 수 있습니다. 전자를 공유함으로써, 두 원자는 공유 전자를 자신의 낙지쪽으로 효과적으로 "수"할 수있다.
* 공유 결합 : 이러한 전자 공유는 공유 결합이라고하는 원자 사이에 강한 인력을 형성합니다.
예 :
물의 예를 들어 보자 :
* 수소 (H) : 원자가 쉘에 1 개의 전자가 있으며 옥셋을 완성하려면 1이 더 필요합니다.
* 산소 (O) : 원자가 쉘에 6 개의 전자가 있으며 옥셋을 완성하려면 2 개가 필요합니다.
2 개의 수소 원자로 2 개의 공유 결합을 형성함으로써 산소는 2 개의 전자를 "공유"하여 옥셋을 완성 할 수 있습니다. 유사하게, 각각의 수소 원자는 하나의 전자를 산소와 "공유"하여 안정적인 구성을 달성 할 수있다.
키 포인트 :
* 공유 결합은 일반적으로 비금속 사이에 형성됩니다.
* 공유 결합의 강도는 공유 전자 쌍의 수에 따라 다릅니다.
* 공유 결합은 공유 전자 쌍의 수에 따라 단일, 이중 또는 삼중 결합 일 수 있습니다.
더 많은 예를 원하거나 공유 결합의 다른 측면을 탐색하고 싶다면 알려주십시오!