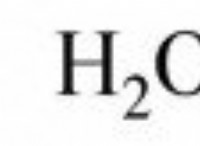다음은 고장입니다.
철 (II) 산화물 (FEO) :
* 양서류 : FEO는 산성 및 기본 특성을 모두 나타내므로 수륙 양용으로 만듭니다.
* 기본 행동 : 염과 물을 형성하기 위해 산과 반응합니다.
* 산성 행동 : 강한베이스와 반응하여 페라이트 (철과 산소를 가진 화합물)를 형성합니다.
철 (III) 산화물 (Fe2O3) :
* 약한 기본 : Fe2O3은 종종 기본으로 간주되지만 상대적으로 약합니다. 산과 반응하여 염과 물을 형성합니다.
* 예 : Fe2O3 + 6HCl → 2FECL3 + 3H2O
철 (II, III) 산화물 (Fe3O4) :
* 혼합 산화물 : Fe3O4는 Fe (II) 및 Fe (III) 이온을 모두 함유하는 혼합 산화물이다. 그 행동은 더 복잡하고 특정 조건에 따라 다릅니다.
산도/염기성에 영향을 미치는 요인 :
* 철의 산화 상태 : 철의 더 높은 산화 상태 (Fe (III))는 산화물을보다 산성으로 만드는 경향이있다.
* 물의 존재 : 물이있는 경우, 산화철은 수산화물을 형성 할 수 있으며, 이는보다 쉽게 기본적입니다.
* 조건 : 주변 환경의 pH에 따라 산도 또는 염기성이 변할 수 있습니다.
기본 특성의 증거 :
* 산과의 반응 : 산화철과 산과의 반응하여 염과 물을 형성하는 것은 그들의 기본 특성을 나타냅니다.
* 수산화물 형성 : 물에서, 산화철은 수산화물을 형성 할 수 있으며, 이는 기본으로 알려져 있습니다.
중요한 참고 :
산화철은 특정 조건에서 기본 특성을 나타낼 수 있지만 특정 산화물과 환경을 고려하는 것이 중요합니다.