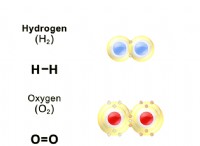
산화물 :
* 정의 : 산소가 다른 원소와 결합 될 때 형성된 화합물.
* 산소 상태 : 산소는 일반적으로 -2 산화 상태에 존재합니다.
* 구조 : 산소 원자는 전형적으로 다른 원자에 개별적으로 결합됩니다.
* 예 : 산화철 (FEO), 이산화탄소 (CO₂), 산화 마그네슘 (MGO)
퍼 옥사이드 :
* 정의 : 단일 결합을 갖는 산소 원자의 이량 체인 과산화수소 이온 (OJER)을 함유하는 화합물.
* 산소 상태 : 산소는 과산화물에서 -1 산화 상태를 갖는다.
* 구조 : 과산화물 이온 (OJET)은 두 산소 원자 사이에 단일 결합을 갖는다.
* 예 : 과산화수소 (HATE), 과산화 나트륨 (NAATERIOM), 바륨 퍼 옥사이드 (BAO₂)
주요 차이점 :
* 산소 상태 : 산화물은 -2 산화 상태에서 산소를 갖는 반면, 과산화물은 -1 산화 상태에서 산소를 갖는다.
* 산소 결합 : 산화물은 산소 원자가 다른 원소에 개별적으로 결합 된 반면, 퍼 옥사이드는 과산화물 이온에서 서로 결합 된 산소 원자가있다 (OJET).
* 반응성 : 과산화물은 일반적으로 산화물보다 반응성이 더 높습니다. 그것들은 강력한 산화제이며 경우에 따라 폭발 할 수 있습니다.
간단히 말해서 :
이런 식으로 생각하십시오 :
* 산화물 : 산소는 "단독"이며 다른 요소에 개별적으로 결합됩니다.
* 퍼 옥사이드 : 산소는 과산화물 이온 (OJomed)에서 "짝을 이루고", 산소 원자 사이의 단일 결합이있다.