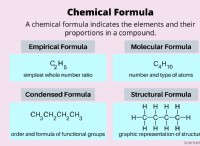
다음은 "자연법"으로 간주 될 수있는 화학에서 이러한 기본 법률의 몇 가지 예입니다.
* 질량 보존 법칙 : 이 법은 일반적인 화학 반응에서 질량을 만들거나 파괴 할 수 없다고 명시하고 있습니다. 이는 화학 반응에서 반응물의 총 질량이 생성물의 총 질량과 동일하다는 것을 의미합니다.
* 명확한 비율의 법칙 : 이 법은 주어진 화학 화합물이 화합물의 공급원에 관계없이 질량에 의해 동일한 비율의 동일한 요소를 항상 함유한다고 말합니다.
* Law of Multiple Proportions: 이 법칙은 두 요소가 하나 이상의 화합물을 형성 할 때, 다른 요소의 고정 질량과 결합하는 한 요소의 질량은 작은 정수의 비율에 있다고 명시하고 있습니다.
* 주기법 : 이 법은 요소의 속성이 원자가의주기적인 기능이라고 명시합니다. 이는 유사한 특성을 가진 요소가 주기율표에서 정기적으로 나타납니다.
* 질량 행동의 법칙 : 이 법은 화학 반응 속도와 반응물의 농도 사이의 관계를 설명합니다. 반응 속도는 반응물의 농도의 생성물에 비례하며, 각각의 화학량 계수와 동일한 전력으로 올라갑니다.
이 법은 단순한 "규칙"이 아니라 원자 및 분자 수준에서 물질이 어떻게 상호 작용하는지를 설명하는 기본 원칙입니다. 그것들은 화학에 대한 우리의 이해의 기초를 형성하며 화학 현상을 예측하고 설명하는 데 중요합니다.
이 맥락에서 "자연법"은 도덕적, 윤리적 원칙을 다루는 철학의 "자연 법"과 동일하지 않다는 점에 주목하는 것이 중요합니다. 화학에서 "자연법"은 물질의 행동을 설명하는 과학적 원칙을 말합니다.