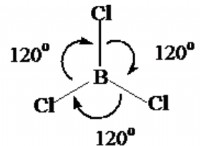
* 루이스 구조 : CO의 루이스 구조는 탄소와 산소 사이의 트리플 결합을 보여줍니다. 이것은 두 개의 시그마 본드와 하나의 PI 본드가 있음을 의미합니다.
* 혼성화 : 탄소 원자는 1 개의 S 및 3 개의 p 궤도를 가지며, 이는 4 개의 SP 궤도를 형성하기 위해 혼성화한다. 이 궤도 중 하나는 산소와 시그마 결합을 형성하는 반면, 다른 3 궤도는 산소와 트리플 결합을 형성합니다.
* 산소 : 산소 원자는 또한 SP 하이브리드 화를 겪고 시그마 결합을 형성하고 탄소와의 PI 결합을 형성한다.
요약 :
* 탄소 원자에는 SP 혼성화가 있습니다.
* 산소 원자에는 SP 혼성화가 있습니다.
이 혼성화는 CO에서 탄소와 산소 사이의 강한 트리플 결합을 형성 할 수있게한다.