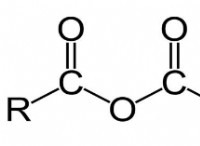
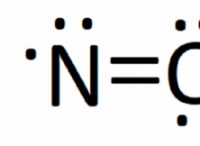so 2 (g) + h 2 o (l) ⇌ h 2 그래서
다음은 어떤 일이 발생하는지에 대한 고장입니다.
* 이산화황 (So
* 물 (H 2 o) 용매 역할을하는 액체입니다.
* 황산 (H 2 그래서
중요한 점 :
* 반응은 가역적이다 : 이것은 황산이 이산화황과 물로 다시 분해 될 수 있음을 의미합니다.
* 황산은 약산이다 : 용액에서만 부분적으로 이온화되므로 모든 수소 이온 (H+)이 방출되지는 않습니다.
* 반응은 산성 비에서 중요하다 : 화석 연료를 태우는 것과 같은 공급원으로부터 대기로 방출되는 이산화황은 빗물에 용해되어 황산을 형성합니다. 이것은 비의 산도에 기여하며, 이는 환경에 유해한 영향을 줄 수 있습니다.
전반적으로, 이산화황과 물 사이의 반응은 산성 비에 기여하는 약산 인 황산의 황산 형성을 초래한다. .