이유는 다음과 같습니다.
* 분자간 힘 : 1- 헥사 놀과 3- 헥사 놀은 알코올이며, 그들의 1 차 분자간 힘은 수소 결합이다. 이것은 끓는점에 크게 기여하는 강력한 힘입니다.
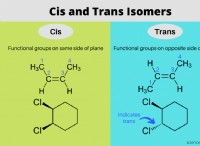
* 분기 : 1- 헥사 놀은 직선형 알코올이고 3- 헥사 놀은 분지됩니다. 분지 분자는 직선형 분자보다 표면적이 낮습니다.
* 감소 된 반 데르 발스 세력 : 분지 분자의 하부 표면적은 약한 반 데르 발스 힘 (분자간 힘의 유형)을 초래합니다.
* 전반적인 영향 : 수소 결합은 둘 다에 존재하지만, 3- 헥사 놀의 약한 반 데르 발스 힘은 분자간 관광 명소를 극복하기 위해 더 적은 에너지가 필요하다.
따라서 3- 헥사 놀의 분지는 1- 헥사 놀보다 더 낮은 비등점으로 이어집니다.