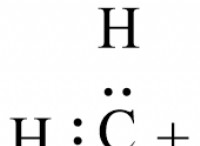가능한 시나리오의 고장은 다음과 같습니다.
1. 중간 가열 (500 ° C 미만)
* 촉매가없는 분해 : 염소산 나트륨은 염화나트륨 (NaCl)과 산소 가스 (O 2 를 형성하기 위해 분해됩니다. ).
* 2naclo 3 (s) → 2NaCl (s) + 3o 2 (g)
2. 고온 (500 ° C 이상)
촉매를 가진 * : 이산화 망염과 같은 촉매의 존재하에 (mno 2 ), 분해는 더 진행된다.
* naClo
*이 반응은 염화나트륨, 산소 가스 및 염소 가스를 생성합니다.
분해에 영향을 미치는 요인 :
* 온도 : 더 높은 온도는 염소 가스의 형성을 선호합니다.
* 촉매 : 이산화 망간은 염소 가스의 생산을 촉진합니다.
* NaClo의 농도 3 : 더 높은 농도의 염소산 나트륨은보다 격렬한 반응을 초래할 수 있습니다.
중요한 메모 :
* 염소산 나트륨의 분해는 매우 발열 반응으로 열을 방출한다는 것을 의미합니다.
* 분해 산물은 위험 할 수 있습니다. 염소 가스는 독성이 있으며 호흡기 시스템에 자극적 일 수 있습니다.
* 항상 염소산 나트륨을 처리하고 안전 절차를 따르십시오.
요약하면, 염소산 나트륨 분해의 1 차 생성물은 염화나트륨과 산소 가스입니다. 그러나 더 높은 온도와 촉매의 존재 하에서는 염소 가스도 생성됩니다.