학위에 수용성이있는 이유는 다음과 같습니다.
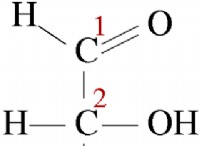
* 극성 : HCN은 수소와 질소 원자 사이에 극성 공유 결합을 갖는다. 이 극성은 물 분자와의 수소 결합을 허용하여 용해도에 기여합니다.
* 작은 크기 : HCN은 소분자로, 물 분자와보다 효과적으로 상호 작용할 수 있습니다.
그러나 여기에 매우 용해되지 않는 이유는 다음과 같습니다.
* 약한 산도 : HCN은 약산으로, 물 분자에 양성자 (H+)를 쉽게 기증하지 않는다는 것을 의미합니다. 이것은 용해도를 향상시킬 강력한 상호 작용의 형성을 제한합니다.
* 독성 : HCN은 매우 독성이 있으며 용해도는 위험에 영향을 미칩니다. 물에 용해되면 생물학적 조직에 더 쉽게 침투하여 피해를 줄 수 있습니다.
요약하면, HCN은 산도가 약하고 작은 크기로 인해 물의 용해도가 제한되어 있습니다. 수소 결합을 통해 물 분자와 상호 작용할 수 있지만, 독성과 약한 산 특성은 가용성이 매우 높지 않습니다.