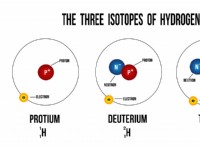
보르의 원자 모델 :단순화 된 그림
1913 년 Niels Bohr가 제안한 Bohr의 원자 모델은 원자의 구조를 설명하는 단순화 된 모델입니다. . 완전히 정확하지는 않지만 원자가 어떻게 행동하는지 이해하는 데 유용한 프레임 워크를 제공합니다.
다음은 주요 기능의 분석입니다.
1. 전자는 "에너지 레벨"이라는 특정 원형 경로에서 핵을 공전합니다.
- 전자가 행성 인 작은 태양계를 태양으로 공전하는 태양계를 상상해보십시오.
-이 궤도는 무작위가 아닙니다. 전자는 각각 별도의 에너지 수준을 갖는 특정 궤도를 차지할 수 있습니다.
2. 에너지 수준은 양자화됩니다.
- 전자는 이러한 특정 에너지 수준에서만 존재할 수 있습니다. 그들은 그들 사이의 공간을 차지할 수 없습니다.
- 이는 전자가 수준 사이의 에너지 차이에 해당하는 특정 양 (Quanta)에서 에너지를 흡수하거나 방출 할 수 있음을 의미합니다.
3. 전자는 빛을 흡수하거나 방출하여 에너지 수준 사이에서 점프 할 수 있습니다.
- 전자가 에너지를 흡수하면 (빛의 광자처럼) 더 높은 에너지 수준으로 점프합니다.
- 전자가 더 낮은 에너지 수준으로 떨어지면 빛의 형태로 에너지를 방출합니다.
4. 핵은 양성자와 중성자를 포함하는 밀도가 높고 양으로 하전 된 중심입니다.
- 핵은 원자의 전체 크기에 비해 작지만 대부분의 질량을 포함합니다.
Bohr의 모델의 강점 :
- 수소 원자의 선 스펙트럼을 설명했는데, 이는 고전 물리학이 설명 할 수없는 주요 관찰입니다.
- 원자의 구조와 상호 작용을 시각화하는 간단한 방법을 제공했습니다.
Bohr 모델의 한계 :
- 수소에만 잘 작동하여 다른 요소의 스펙트럼을 정확하게 예측하지 못했습니다.
- 원자 사이의 화학적 결합을 설명 할 수 없었습니다.
- 분자의 모양과 원자의 외부 영역에서 전자의 거동을 설명 할 수 없었습니다.
요약하면, Bohr의 모델은 기본 원자 개념을 이해하기위한 귀중한 도구이지만 원자의 완전히 정확한 그림은 아닙니다. 양자 기계 모델과 같은 후속 모델은 원자 행동에 대한보다 상세하고 정확한 설명을 제공했습니다.