금속 + 산 → 염 + 수소 가스
예 :
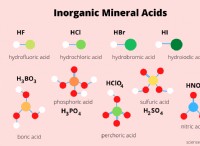
딜 루트 염산 (HCL)과 마그네슘 (MG)의 반응
mg (s) + 2hcl (aq) → mgcl₂ (aq) + h₂ (g)
설명 :
* mg (s) : 고체 상태의 마그네슘 금속.
* 2hcl (aq) : 수성 용액에서 하이드로 클로르 산.
* mgcl> (aq) : 클로라이드 마그네슘, 염은 수용액으로 형성되었다.
* h₂ (g) : 반응의 생성물 인 수소 가스는 가스로 방출됩니다.
참고 :
* 이것은 단일 변위 반응으로, 더 반응성 금속 (마그네슘)은 산으로부터 덜 반응성 수소를 대체합니다.
* 생산 된 수소 가스는 용액에서 기포로 관찰 될 수 있습니다.
* 형성된 특정 염은 사용 된 금속과 산에 따라 다릅니다. 예를 들어, 아연을 황산과 반응 시키면 황산 아연을 생성 할 수 있습니다.
일반적인 고려 사항 :
* 모든 금속이 산과 반응하는 것은 아닙니다. 금속의 반응성은 다양하며 일부는 산 공격에 더 저항력이 있습니다.
* 산의 농도는 반응 속도에 영향을 미칩니다.
* 반응은 발열이 될 수 있으므로 열이 방출됩니다.
이것은 일반적인 표현이라는 점에 유의해야하며, 특정 균형 방정식은 관련된 반응물에 따라 다릅니다.