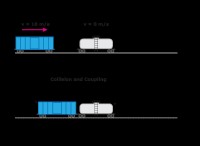
1. 합성 반응 (조합 반응) :
* 정의 : 둘 이상의 반응물이 결합되어 단일 생성물을 형성합니다.
* 일반 양식 : A + B → AB
* 예 : 2 Na (S) + Cl s (G) → 2 NaCl (S) (나트륨 및 염소 가스로부터 염화나트륨의 형성)
2. 분해 반응 :
* 정의 : 단일 반응물은 둘 이상의 단순한 제품으로 분해됩니다.
* 일반 양식 : AB → A + B
* 예 : CACO₃ (S) → CAO (S) + CO₂ (G) (탄산 칼슘의 산화 칼슘 및 이산화탄소로의 분해)
3. 단일 및 이중 변위 반응 :
* 정의 : 두 반응물의 원자 또는 이온은 장소를 전환합니다.
* 단일 변위 : 한 요소는 화합물에서 다른 요소를 대체합니다.
* 일반 양식 : A + BC → AC + b
* 예 : Zn (s) + cuso₄ (aq) → znso₄ (aq) + Cu (S) (아연은 황산 구리의 구리를 대체 함)
* 이중 변위 : 두 개의 화합물 교환 이온.
* 일반 양식 : AB + CD → AD + CB
* 예 : agno₃ (aq) + NaCl (aq) → agcl (s) + nano₃ (aq) (질산은 및 염화나트륨 반응하여은 염화물 침전물 및 질산 나트륨을 형성하기 위해 반응)
이러한 범주는 상호 배타적이지 않으며 많은 반응이 여러 범주에 속할 수 있습니다. 또한, 이러한 기본 범주를 기반으로하는 연소, 중화 및 산화 환원 반응과 같은 다른 많은 특정 유형의 반응이 있습니다.