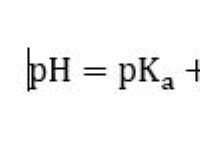이유는 다음과 같습니다.
* 알루미늄 (Al)에는 3 개의 원자가 전자가 있습니다. 3 개의 불소 (F) 원자로 3 개의 단일 결합을 형성합니다.
* 불소 (F)에는 7 개의 원자가 전자가 있습니다. 각각의 F 원자는 Al과 단일 결합을 형성하고 3 개의 고독한 전자 전자를 갖는다.
* Al 원자에는 3 개의 결합 쌍과 1 개의 고독한 전자 쌍이 있습니다. 이것은 중앙 원자 주위에 총 4 개의 전자 쌍을 제공합니다.
* 4 개의 전자 쌍이 전자 반발을 최소화하기 위해 사면체 모양으로 자신을 배열합니다.
전자 쌍 형상은 사면체이지만, 분자 형상 Alf3의 trigonal 평면 이다 Al 원자의 고독한 쌍은 모양에 기여하지 않기 때문입니다.