1. 원자 궤도 :
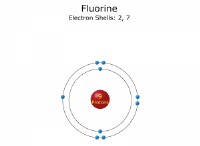
* 탄소 : 전자 구성 1s² 2s² 2p²가 있습니다. 우리는 주로 2S 및 2P 궤도에 관심이 있습니다.
* 산소 : 전자 구성 1s² 2s² 2p⁴입니다. 다시, 우리는 2s 및 2p 궤도에 중점을 둡니다.
2. 분자 궤도 :
* σ 결합 궤도 : 탄소 및 산소 둘 다의 2S 궤도는 에너지가 더 낮은 σ 결합 궤도 (σ2S)를 형성하고 에너지가 더 높은 σ* 안티 본딩 궤도 (σ* 2s)를 형성합니다.
* σ 및 π 결합 궤도 : 탄소 및 산소 둘 다의 2P 궤도는 결합되어 2 개의 더 결합 궤도를 형성한다. 하나는 σ 결합 궤도 (σ2p)이고 다른 하나는 π 결합 궤도 (π2p)입니다.
* π 항비 궤도 : 2P 궤도는 또한 2 개의 π 항의 궤도 (π*2p)를 형성한다.
3. 분자 궤도를 채우기 :
* 총 원자가 전자 : 탄소는 4 개의 원자가 전자에 기여하고 산소는 6을 기여하여 총 10 개의 원자가 전자가 분자 궤도를 채 웁니다.
* 충전 순서 : 분자 궤도는 에너지 증가 순서대로 채워집니다.
* σ2s
* σ* 2s
* σ2p
* π2p
* π* 2p
분자 궤도 다이어그램 :
```
-------------------- π*2p (안티본 딩)
| |
-------------------- σ*2p (안티본 딩)
| |
-------------------- π2p (본딩)
| |
------------------- σ2p (본딩)
| |
-------------------- σ*2S (안티본 딩)
| |
------------------- σ2S (Bonding)
C o
```
주요 관찰 :
* 채권 명령 : 결합 순서는 [(결합 전자 수) - (안티 본딩 전자의 수)] / 2로 계산됩니다. CO에는 8 개의 결합 전자와 2 개의 항 바이 본딩 전자가있어 3의 결합 순서를 제공합니다. 이는 매우 강한 트리플 결합을 나타냅니다.
* 파라 마그네즘/디아 마그네틱 : CO는 모든 전자를 짝을 이루어 디아마그네틱하게 만듭니다.
* 전기 음성 : 산소는 탄소보다 전기 음성입니다. 이것은 결합 궤도의 전자 밀도가 산소 원자쪽으로 약간 이동하여 산소에 부분적 음전하와 탄소에 부분 양전하를 만듭니다.
다른 질문이 있으면 알려주세요.