처음에 :
* 버퍼링 용량 : 완충액은 소량의 산 또는 염기가 첨가 될 때 pH의 변화를 방지합니다. 이것은 약산 및 그의 컨쥬 게이트 염기 (또는 약한 염기 및 그의 컨쥬 게이트 산)를 함유하기 때문이다.
* pH 안정성 : 버퍼 용액의 pH는 소량의 산을 첨가함에 따라 비교적 안정적으로 유지됩니다.
더 많은 산 :
* 버퍼링 용량 감소 : 첨가 된 산을 중화시키는 완충제의 능력은 감소한다. 약산의 농도는 증가하는 반면, 접합체 염기의 농도는 감소한다.
* pH 변화 : 용액의 pH는 더 빠르게 감소하기 시작합니다 (더 산성이됩니다).
버퍼링 용량 이상 :
* 버퍼가 소진 : 결국, 첨가 된 산을 중화시키는 완충 용량은 완전히 소진된다. 컨쥬 게이트 염기의 농도는 매우 낮아집니다.
* 빠른 pH 드롭 : 그런 다음 PH는 부러되지 않은 용액의 거동과 유사한 산의 각 첨가에 따라 크게 떨어질 것입니다.
요약 :
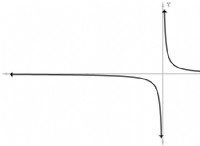
* 버퍼 용액에 산을 첨가하면 처음에는 pH의 작은 변화가 발생합니다.
* 더 많은 산 첨가함에 따라 pH 변화가 더욱 두드러집니다.
* 결국, pH 변화에 저항하는 버퍼의 용량은 압도 당하고 pH는 빠르게 떨어집니다.
예 :
아세트산 (ch₃cooh)과 아세테이트 이온 (Ch₃coo⁻)을 함유 한 완충액을 상상해보십시오. 산 (h ()을 첨가하면 다음 반응이 발생합니다.
ch₃coo⁺ + h⁻ ⇌ ch₃cooh
초기에, 아세테이트 이온은 첨가 된 수소 이온과 쉽게 반응하여 pH의 변화를 최소화한다. 그러나, 더 많은 산 첨가함에 따라, 아세테이트 이온의 농도는 감소하고, 첨가 된 산을 중화시키는 완충 용량은 감소한다.